Компьютерная томография и биомеханическое сопровождение в челюстно-лицевой хирургии с использованием комплекса Mimics-Ansys
А. Н. Чуйко
к. т. н., доцент (Харьков, Украина)
Р. А. Левандовский
к. м. н., доцент кафедры терапевтической и ортопедической стоматологии Буковинского государственного медицинского университета (Черновцы, Украина)
Д. К. Калиновский
к. м. н., доцент кафедры хирургической стоматологии Донецкого национального медицинского университета им. М. Горького (Украина)
Д. А. Грибов
аспирант кафедры «Прикладная механика» Московского государственного технического университета им. Н. Э. Баумана
Введение
Эффективность системы CT/CAD/CAE/CAM при биомеханическом сопровождении операций в челюстно-лицевой хирургии с конкретной реализацией возможностей, заложенных в программах MIMICS и SolidWorks, достаточно подробно рассмотрена в работах [3, 4]. При 3D-визуализации и сегментации большими возможностями обладает программа MIMICS; при проектировании и подгонке имплантатов на основе виртуальных STL-моделей рационально использовать комплекс MIMICS-SolidWorks.
Эти возможности показаны в первой части работы [4] на конкретных клинических примерах. Во второй части работы [4] проведены расчеты на прочность и жесткость по приближенной методике, использующей общие закономерности механики, но неоднократно подчеркнуто, что более точно такие расчеты следует проводить на основе конечно-элементного моделирования и анализа. Только такой, более глубокий анализ, соответствующий современному развитию науки, позволит ответить на вопросы о рациональности и долговечности проведенной реконструкции.
Целью предлагаемого исследования, представляющего собой логическое продолжение работ [3, 4], является демонстрация возможностей комплекса MIMICS-ANSYS при анализе механических свойств костных и мягких тканей и конечно-элементном анализе проведенной реконструкции нижней челюсти пациента.
Материал и методы
Как отмечено во введении и в работах [3, 4], конечно-элементное моделирование и анализ в медицине получают новые практически неограниченные возможности, если оно строится на базе компьютерной томографии. Появляется возможность строить не канонические или идеализированные модели, а модели, максимально приближенные к конкретному пациенту как по геометрии, так и по свойствам мягких и костных тканей, практически получая модель in vivo.
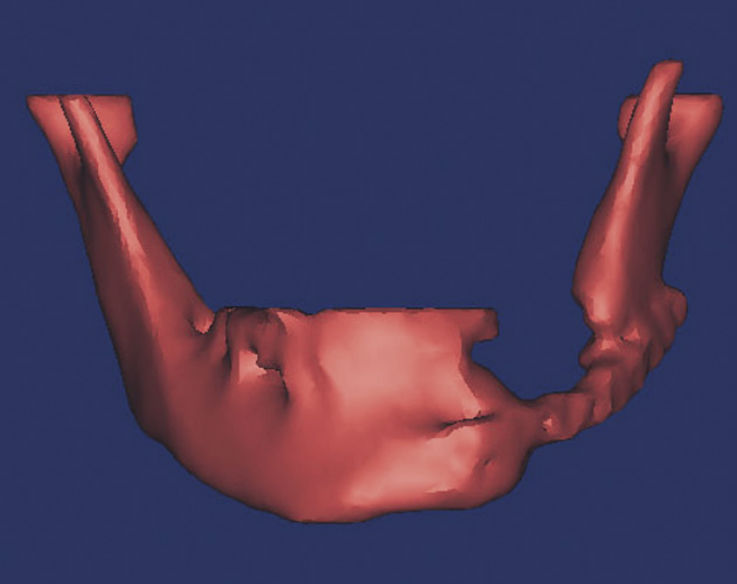
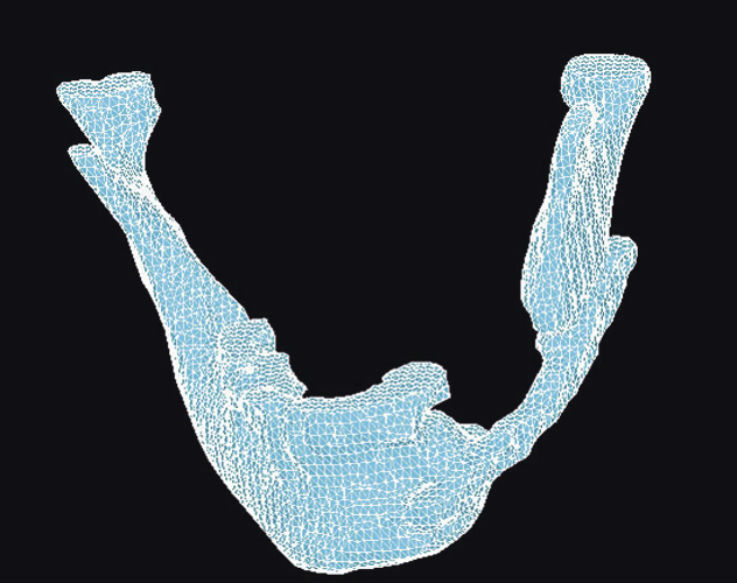
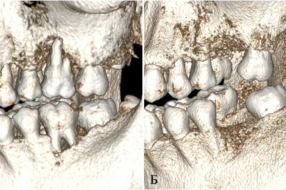
Рассмотрим возможности комплекса MIMICS-ANSYS на примере операции пациента К. [4]. Сегментированная НЧ после контрольной CT и после сглаживания в программе MIMICS показана на рис. 1, а на рис. 2 один из вариантов конечно-элементного разбиения в ANSYS. Одним из достоинств комплекса MIMICS-ANSYS является возможность назначать свойства материалов анализируемого объекта на основе чисел Хаунсфилда HU (или GV).
Если мы не знаем количественных механических (прочностных) характеристик кости (конструкционных материалов) конкретного пациента, то все наши рассуждения будут носить качественный характер — нужно больше, нужно меньше. До недавнего времени вопрос о механических свойствах костных тканей конкретного пациента в режиме реального времени оставался неразрешимым. Это объясняется большой сложностью, а часто и невозможностью проведения прямых испытаний костных тканей in vivo. В научных исследованиях использовались статистические данные, полученные с применением косвенных методов (ультразвуковые, замер твердости и т. п.), которые, как правило, даются в широких пределах без дифференциации по полу, возрасту и виду заболевания.
Ситуация изменилась кардинальным образом после создания компьютерной томографии (CT), которая, помимо возможностей по диагностике, заложила основу разработки методики по калибровке чисел Хаунсфилда (Haunsfield, HU) в реальную плотность кости, что позволяет получать основные механические характеристики (предел прочности, модуль упругости) костных тканей пациента фактически в режиме реального времени. Появляется возможность построения карты плотности костных и мягких тканей, в первую очередь, в зонах, где предполагается размещение опорных элементов протеза, имплантата и фиксирующих элементов.
Программа MIMICS [5] позволяет определить основные механические характеристики мягких и костных тканей фактически в режиме in vivo, по эмпирическим формулам, зависящим от типа рассматриваемой ткани. Для компактной кости Femur рекомендуются следующие формулы.
Для определения плотности ρ или DN (Density)
DN = -13,4 + 1017 GV (1),
где GV (Grey Values) — значения серого на томограмме.
Значение модуля упругости E вычисляется по формуле
E = 388,8 + 5925 DN (2).
Результаты расчетов по этим формулам во всем диапазоне значений серого приведены на рис. 3 — штрихпунктирная линия.

Рис. 3. Значения модуля упругости (по разным источникам), предела прочности и плотности тканей в зависимости от оттенков серого
В разных литературных источниках [5, 7] приводятся различные соотношения для определения основных механических характеристик костных тканей — модуля упругости Е и предела прочности σ в зависимости от плотности. На рис. 3 для графических зависимостей σ и Е использованы эмпирические формулы [7]
E = 2195 ρ3 и σ = 60 ρ2 (3),
где ρ — плотность костной ткани, которая измеряется в г/см³.
В этом случае модули упругости и напряжения имеют размерность мегапаскаль (MPa). Как видим, при плотности кости ρ около 1,8 г/см³ эти кривые пересекаются, т. е. значения совпадают.
На рис. 4. в таблице приведены численные значения свойств материалов — плотности, модуля упругости и коэффициента Пуассона по группам.
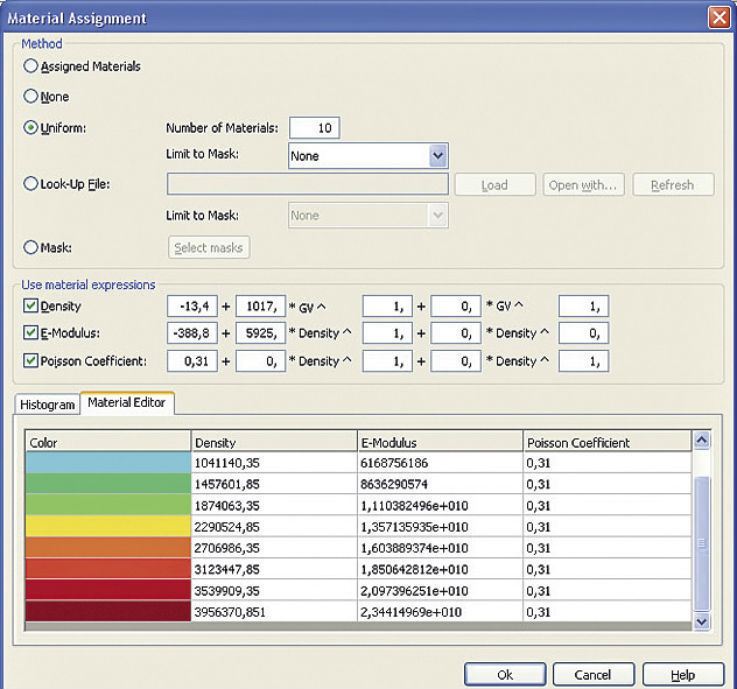
Рис. 4. Численные значения свойств материалов — плотности, модуля упругости и коэффициента Пуассона по группам
Полученные результаты кратко прокомментируем.
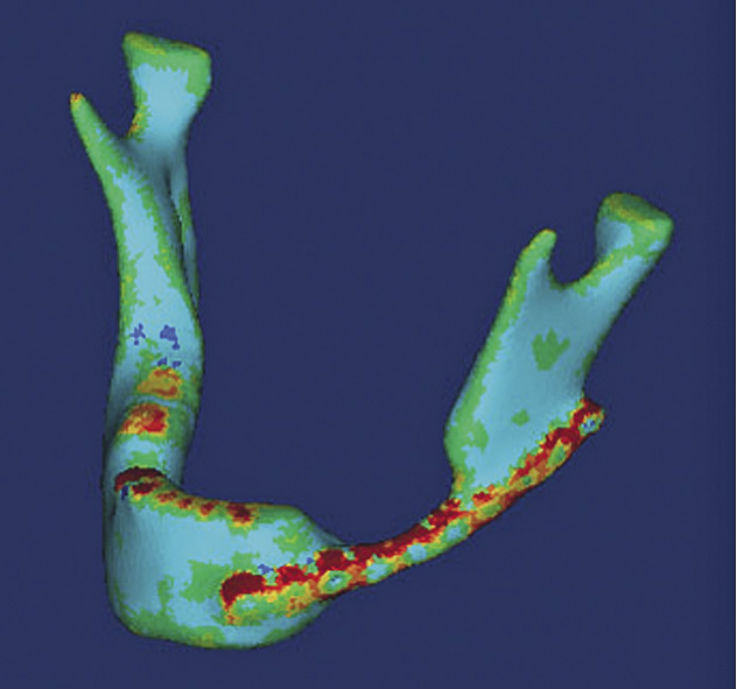
Во-первых, налицо «обволакивание» имплантата достаточно плотной костной тканью, что в [4] объяснялось как развитие процессов остеоинтеграции. Особенно это явление заметно в зонах отверстий в имплантате и расположения фиксирующих винтов.
Во-вторых, как следует из рис. 3 и зависимости (1), верхний предел фиксируемой плотности кости ρ = 4,16 г/см³, т. е. модуль упругости по соотношению (2) не может быть выше, чем E = 2,47∙1010 Па. Но у титана, материала, из которого выполнен пластинчатый имплантат, модуль упругости E = 1,1∙1011 Па, т. е. в 4,5 раза выше.
Преодоление этого затруднения можно реализовать в программе ANSYS, в которой происходит такое же, как в таблице на рис. 4, распределение свойств материалов по группам. Но для группы с самым высоким модулем упругости это значение можно изменить «вручную», заменив на соответствующее число, равное модулю упругости титана. На наш взгляд, такой подход позволяет учесть механические свойства имплантата и в рамках версии MIMICS10, которая не поддерживает создание неоднородных сборок.
Результаты и их обсуждение
Анализ напряженно-деформированного состояния НЧ с использованием комплекса MIMICS-ANSYS.
Далее проведем оценку напряженно-деформированного состояния нижней челюсти пациента К при различных моделирующих процесс откусывания и жевания пищи (рис. 6, 7) условиях нагружения, следуя расчетным схемам, представленным во второй части [4].
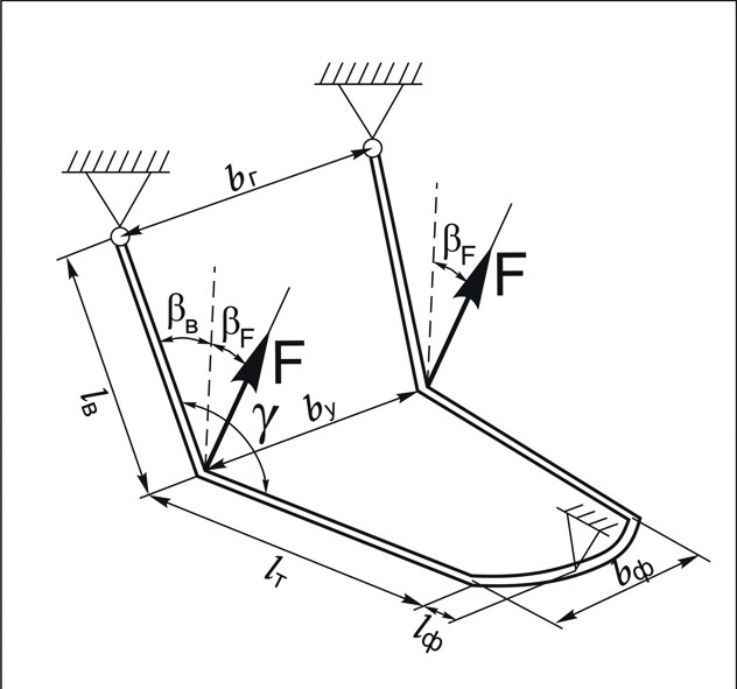
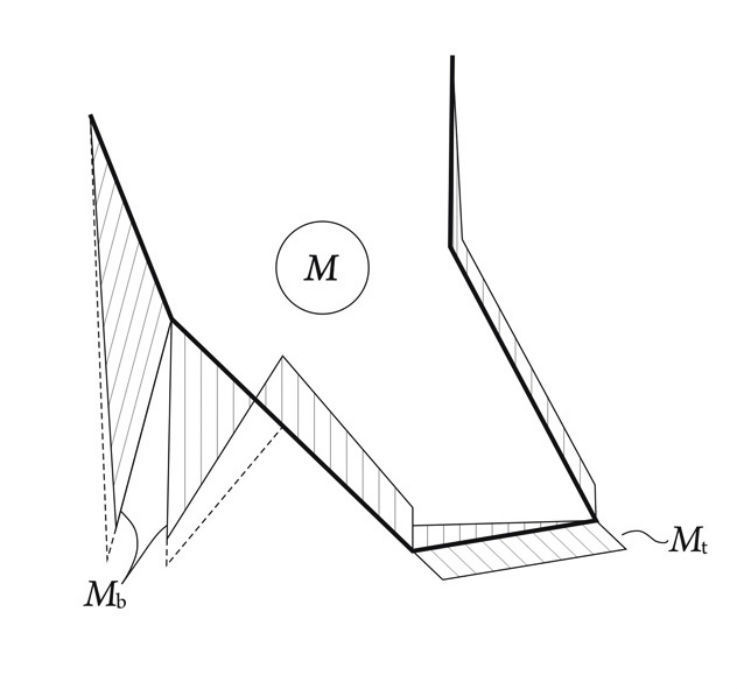
Так как биомеханическому анализу процесса откусывания пищи посвящен практически целый раздел [4], схематически, следуя [3], рассмотрим и процесс одностороннего жевания, приложив жевательную нагрузку к правому углу челюсти. Эпюра изгибающих и крутящих моментов для этого случая приведена на рис. 8.
Эпюра на рис. 8 демонстрирует важный для практических приложений вывод [3]. Несмотря на то что при разжевывании пищи сила, развиваемая жевательной мышцей, более чем в 5 раз превышает силу при откусывании, изгибающие моменты, возникающие в теле нижней челюсти, практически не изменяются (из-за изменения плеч передачи нагрузки). В этом, можно предполагать, и состоит «мудрость» эволюции.
Далее приступим к непосредственному моделированию. На рис. 9 показан общий вид конечно-элементной модели с учетом распределения свойств тканей и ее разрез в сагиттальной плоскости и один из вариантов сетки МКЭ в ANSYS. Модель содержит 83 236 узлов и 451 367 элементов типа SOLID72. Некоторое различие в цветовой гамме на рис. 5 и 7 объясняется ограничением количества цветов в программе ANSYS.
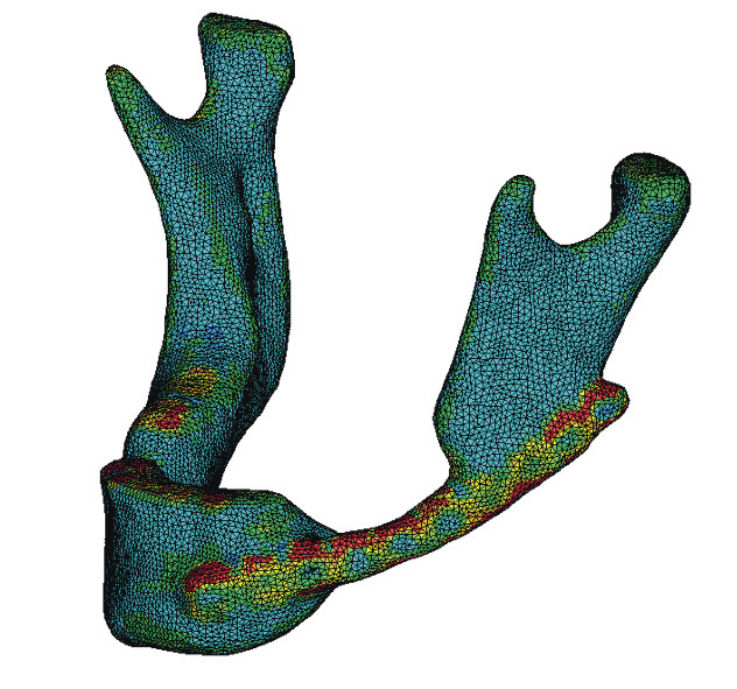
Рис. 9а. Общий вид конечно-элементной модели с учетом распределения свойств тканей и ее разрез в сагиттальной плоскости
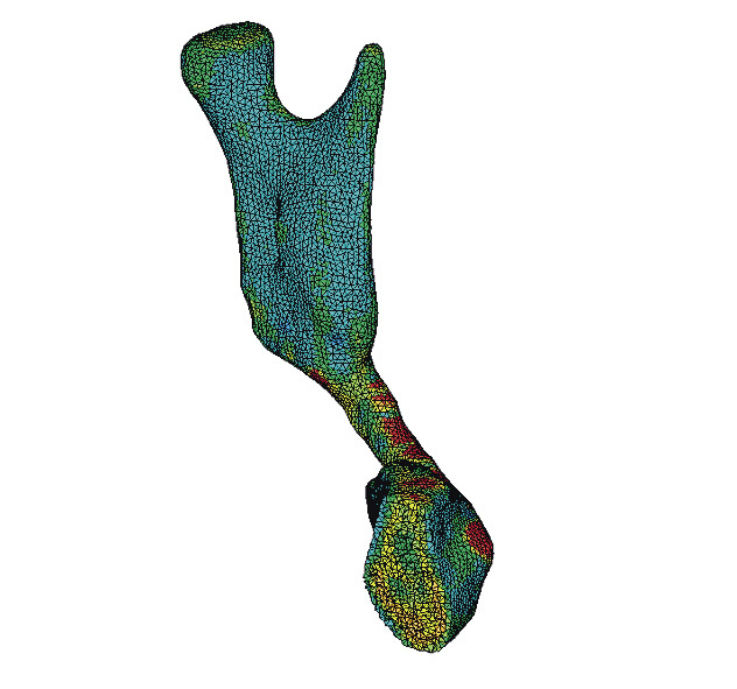
Рис. 9б. Общий вид конечно-элементной модели с учетом распределения свойств тканей и ее разрез в сагиттальной плоскости
На рис. 10 и 11 представлены модели, отражающие процесс откусывания и жевания пищи, на которых условно показаны нагрузка и граничные условия.
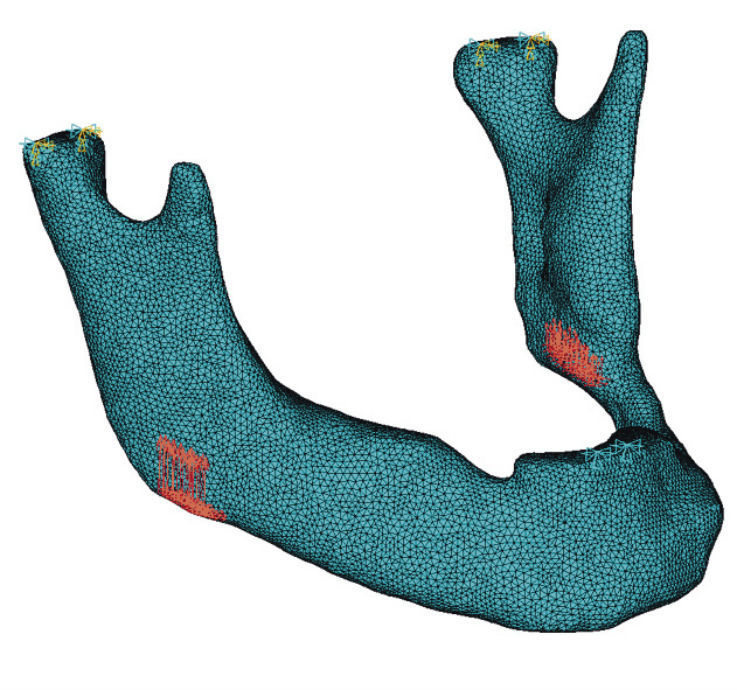
Рис. 10. Конечно-элементная модель с приложенными граничными условиями и нагрузками при откусывании пищи
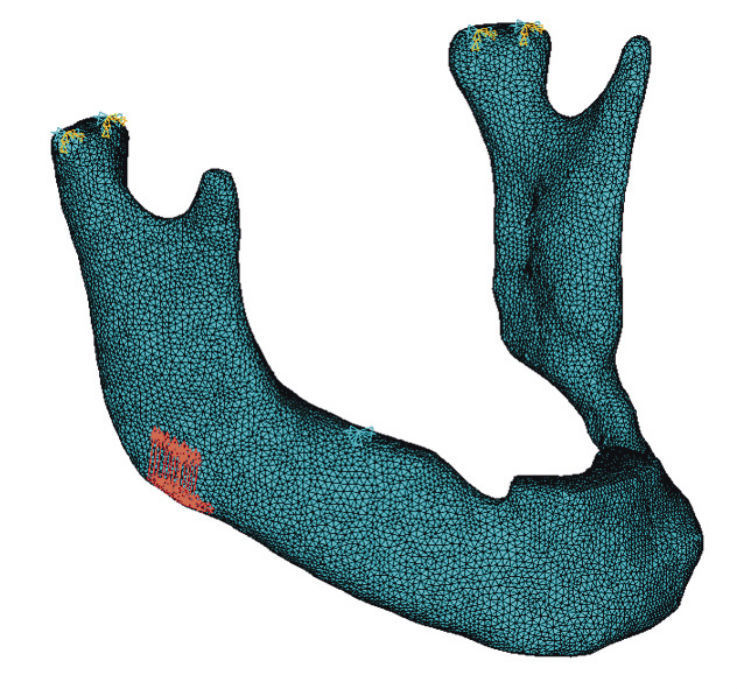
Рис. 11. Конечно-элементная модель с приложенными граничными условиями и нагрузкой при одностороннем жевании пищи
Подчеркнем кратко особенности этих моделей и их различия. Как подчеркивалось при обсуждении расчетных схем [3, 4], головки НЧ являются естественными шарнирами, а сама НЧ — механизмом до контакта с любым зубом-антагонистом или пищевым комком. При откусывании пищи в роли зубов-антагонистов, препятствующих вращению челюсти, выступают резцы (рис. 8), а при одностороннем жевании — моляр (рис. 9).
Учитывая, что вращение головки происходит вокруг ее наружной поверхности, находящейся в контакте с диском ВНЧС, на каждой головке (рис. 10, 11) намечено по два узла, в которых отсутствуют все линейные перемещения и возможно только одно угловое перемещение вокруг оси, проходящей через эти узлы, т. е. UX = UY = UZ = ROTY = ROTZ = 0. На рис. 10 и 11 эти узлы обозначены желто-зелеными треугольниками. Зубы-антагонисты, препятствующие вращению НЧ, лишены только линейных перемещений, то есть UX = UY = UZ = 0. На рис.10 и 11 они обозначены светло-зелеными треугольниками — в зоне резцов и правого моляра. Такие граничные условия позволяют отразить все возможные деформации изгиба и кручения НЧ.
Жевательная нагрузка прикладывается к углу челюсти в виде распределенной на небольшом участке (в месте прикрепления жевательной мышцы) под углом 30˚ к вертикали относительно тела НЧ и ориентирована вдоль ветви челюсти, что обеспечивается разложением ее вектора на три составляющих Fx, Fy и Fz. При откусывании пищи вектор силы по F = 150Н (соответственно, Fx = 34,3Н, Fy = 66,7Н и Fz = 129,9Н) прикладывается к обоим углам челюсти симметрично. При жевании пищи вектор силы F = 200 Н (соответственно, Fx = 45,8Н, Fy = 88,9Н и Fz = 173,2Н) прикладывается к правому углу челюсти, т. е. несимметрично. Так как задача решается в линейной постановке, полученные ниже результаты могут быть интерполированы (пропорционально) для любых нагрузок.
Результаты расчета основных параметров НДС НЧ представлены на рис. 12—15.
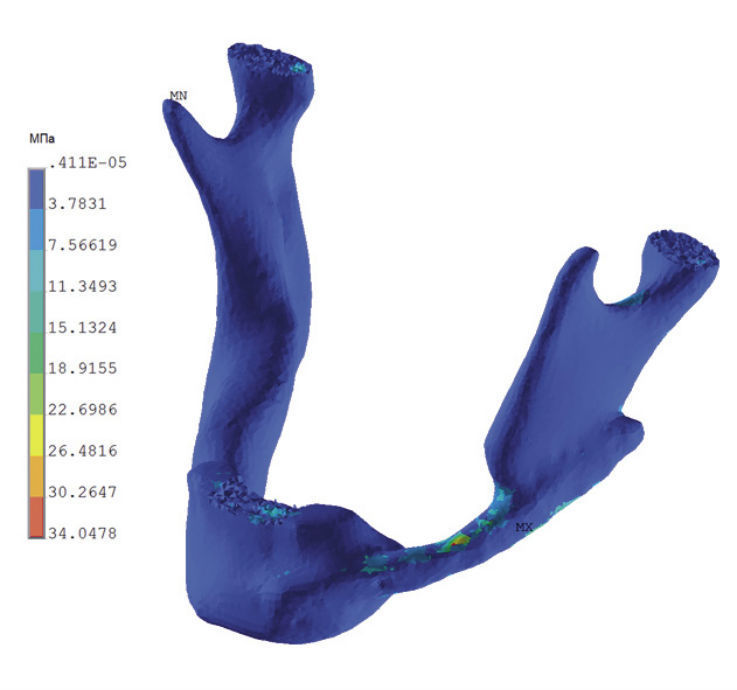
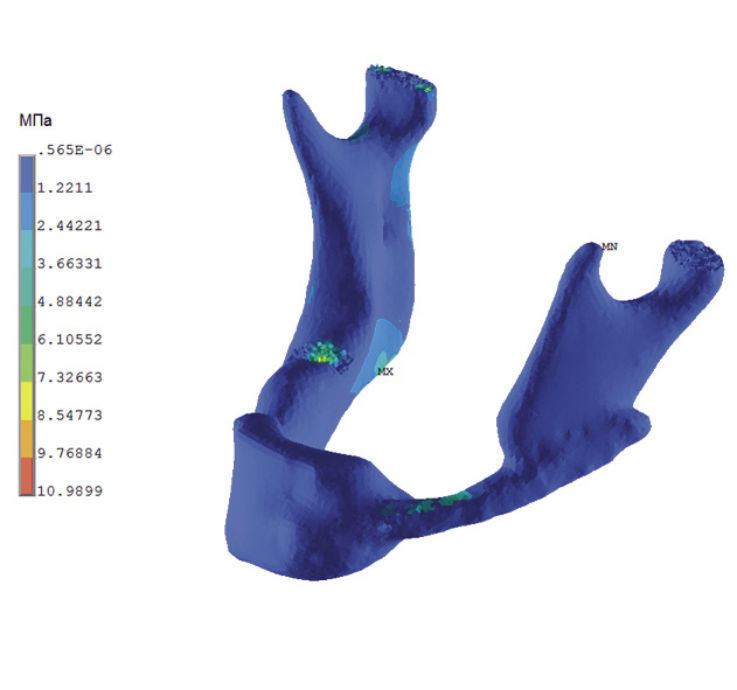
На рис. 12 и 13 показаны поля эквивалентных напряжений (по Мизесу) при откусывании и жевании пищи, соответственно, при жевательной нагрузке, обозначенной выше.
Как отмечалось выше, максимальные изгибающие моменты как при откусывании пищи, так и при одностороннем жевании возникают в зоне угла челюсти. Но в этой же зоне кость НЧ имеет максимальный момент сопротивления за счет большого вертикального размера и высокой плотности кости. Именно в силу этих факторов коэффициент запаса прочности нижней челюсти достаточно велик (как показано в [4], у пациента Л в норме (до операции) при откусывании равен 26,3). Абсолютные значения напряжений по Мизесу в зонах концентрации напряжений значительно ниже травмирующих (допускаемых) напряжений для кости. Эти цифры объясняют, почему обычный человек при нагрузках, близких к норме, проблем с прочностью и жесткостью челюсти не испытывает как в режиме откусывания и жевания, так и при занятиях спортом и бытовых нагрузках.
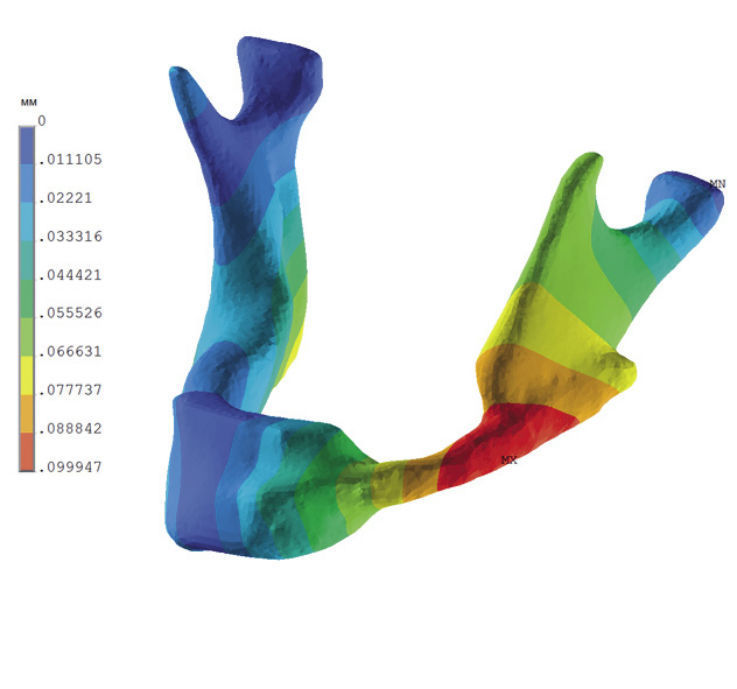
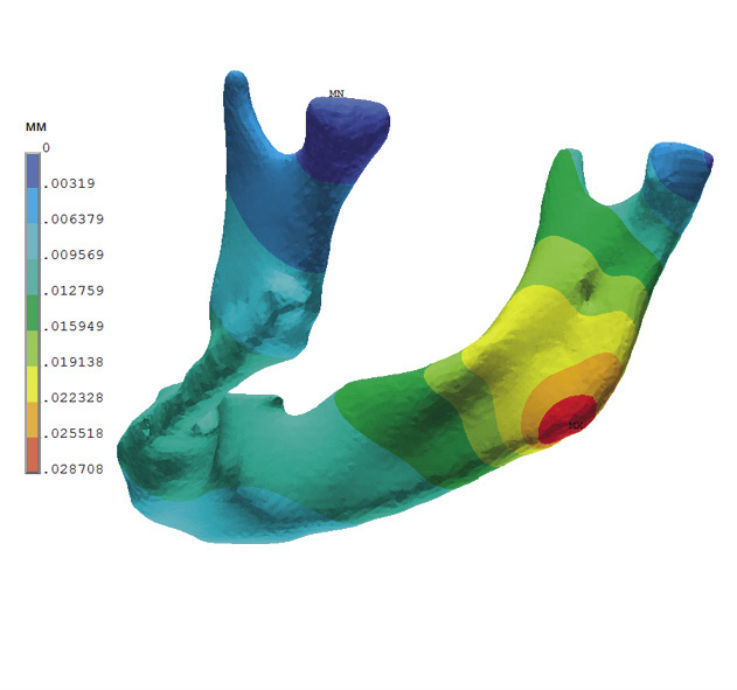
На рис. 14 и 15 показаны поля суммарных перемещений для рассматриваемых расчетных случаев. Подчеркнем, что поля суммарных перемещений носят «ожидаемый» характер, объясняемый и особенностью «конструкции» рассматриваемой челюсти, и граничными условиями, и характером прикладываемых нагрузок. Как следует из сравнения цветных диаграмм на рис. 14 и 15, при откусывании пищи перемещение левого угла челюсти в 3,48 раза больше, чем при одностороннем жевании. Но абсолютные цифры, равные, соответственно, 0,0999 и 0,0287 мм, характеризующие суммарное перемещение угла челюсти, очень небольшие и практически пациентом ощущаться не могут.
Учитывая, что полученные величины напряжений и перемещений при нагрузках, близких к норме, проблем у пациента К вызывать не должны, рассмотрим более детально возможную критическую зону — зону сочленения имплантата с костью. На рис. 16 приведены поля напряжений по Мизесу в имплантате, а на рис. 17 — распределение модуля упругости в имплантате и слоях, примыкающих к фиксирующим винтам.
Подчеркнем, что поля напряжений, представленные на рис. 12, 13 и 16, — это действующие напряжения, величины которых, в соответствии с условием прочности, необходимо сравнивать с травмирующими (допускаемыми) напряжениями.
Максимальные значения напряжений в имплантате значительно ниже принятого выше предела усталостной прочности для титана. Вообще, исследование прочности и жесткости имплантата (определение его конструктивных параметров) как металлической детали затруднений не вызывает, так как здесь могут быть использованы все известные методы сопротивления материалов и деталей машин.
Сложнее выглядит вопрос с соблюдением условия прочности в костных тканях, особенно в слоях, примыкающих к фиксирующим винтам. Кроме определения величины действующих напряжений, необходимо иметь достоверную методику оценки травмирующих (допускаемых) напряжений, например как представленную зависимостью (3) и ее графической интерпретацией на рис. 3. Вопрос этот предполагается исследовать дополнительно, так как именно эта зона может стать местом развития резорбции костной ткани с последующим ослаблением фиксирующих винтов и увеличением подвижности имплантата.
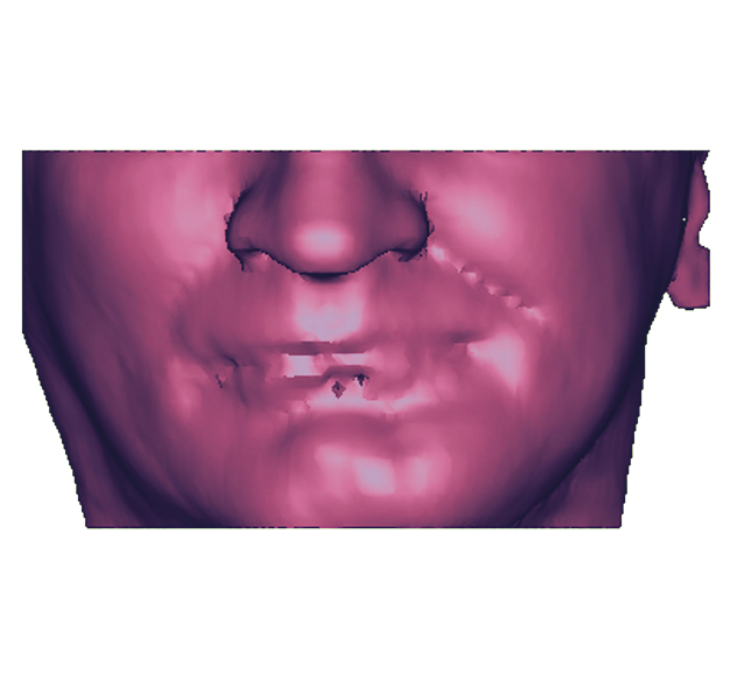
Таким образом, уточненный анализ основных параметров НДС НЧ пациента К. по данным контрольной томографии опасений, высказанных в [4] при предварительном анализе, не подтвердил. На рис. 18 представлена лицевая часть пациента К. после контрольной томографии.
Последующие после контрольной томографии осмотры пациента К. показали, что его состояние удовлетворительное, имплантат «не прорезался», функция НЧ вполне адекватна прикладываемым нагрузкам.
Выводы и практические рекомендации
- Показана эффективность системы CT/CAD/CAE/CAM при биомеханическом сопровождении операций челюстно-лицевой хирургии с конкретной реализацией возможностей, заложенных в программах MIMICS, SolidWorks и ANSYS. При 3D-визуализации и сегментации большими возможностями обладает программа MIMICS; при проектировании и подгонке имплантатов на основе виртуальных STL-моделей рационально использовать комплекс MIMICS-SolidWorks; при анализе механических свойств костных и мягких тканей и конечно-элементном анализе целесообразно использовать комплекс MIMICS-ANSYS.
- Расчеты на прочность и жесткость либо по приближенной методике, либо более точно, на основе конечно-элементного моделирования и анализа, позволяют ответить на вопросы о рациональности и долговечности проведенной реконструкции.
- Следует ожидать существенных изменений в уровне подготовки и характере работы черепно-челюстно-лицевых хирургов с опорой на современные компьютерные технологии. Для биомеханического обоснования принимаемых решений, особенно на этапе планирования операции, в бригаду должен входить специалист, владеющий основами биомеханики хотя бы в степени, достаточной для проведения необходимых расчетов.
- Предлагаемая система CT/CAD/CAE/CAM может быть использована челюстно-лицевыми хирургами, стоматологами-ортопедами, имплантологами, ортодонтами, травматологами-ортопедами и др.: она позволяет моделировать любые элементы реконструкции, не вскрывая предварительно операционное поле.
- Алямовский А. А. SolidWorks 2007/2008. Компьютерное моделирование в инженерной практике / Алямовский А. А. — СПб.: БХВ-Петербург, 2008. — 1040 с.: ил.
- Басов К. А. ANSYS: справочник пользователя. — М.: ДМК Пресс, 2005. — 640 с., ил.
- Чуйко А. Н., Шинчуковский И. А. Биомеханика в стоматологии: Монография. — Х.: Изд-во «Форт». 2010. — 516 с., ил.
- Чуйко А. Н., Калиновский Д. К., Пограничная К. Р., Алымбаев Р. С. О возможностях и некоторых результатах биомеханического сопровождения в челюстно-лицевой хирургии // Дентал Юг. — 2011, № 10 — С. 8—15; № 11. — С. 40—45.
- Mimics 12. Пакет обработки изображений. Базовый обучающий курс. — Materialise, 2008. — С. 82.
- Chuiko A. N., Kalinovsky D. K., Matros-Taranets I. N., Dufash I. K. The peculiarities of biomechanics of the mandible during osteosynthesis with bone-borne plates with screws. Journal of Biomechanics 2006; Vol. 39 Suppl. 1, p. S. 565.
- Mow C., Hayes W. C. Basic Orthopedic Biomechanics, New York 1991.