Использование воздушно-абразивных технологий для консервативной терапии воспалительных заболеваний пародонта
Р. Т. Буляков
д. м. н., доцент, заведующий кафедрой стоматологии общей практики ИПО БГМУ, главный внештатный стоматолог Министерства здравоохранения Республики Башкортостан, заслуженный врач Республики Башкортостан, главный врач АУЗ «Республиканская стоматологическая поликлиника» (Уфа)
О. А. Гуляева
к. м. н., ассистент кафедры стоматологии общей практики ИПО БГМУ, врач- пародонтолог АУЗ «РСП» (Уфа)
Д. Н. Тухватуллина
к. м. н., доцент кафедры стоматологии общей практики ИПО БГМУ, заместитель главврача по лечебной части АУЗ «РСП» (Уфа)
Р. И. Сабитова
врач-стоматолог АУЗ «РСП» (Уфа)
Т. С. Чемикосова
к. м. н., доцент кафедры терапевтической стоматологии ИПО БГМУ, заслуженный врач Республики Башкортостан
М. И. Гумерова
к. м. н., доцент кафедры стоматологии общей практики ИПО БГМУ, заведующая лечебно-профилактичеким отделением платных услуг АУЗ «Республиканская стоматологическая поликлиника» (Уфа)
Воспалительные заболевания пародонта (ВЗП) являются наиболее распространенным заболеванием взрослого населения мира. По результатам обследования 53 стран, согласно данным Всемирной организации здравоохранения, наиболее высокий уровень заболеваемости пародонтитом приходится на возраст 35—44 лет (65—98 %) [10]. Комплексное эпидемиологическое стоматологическое обследование в 40 регионах России показало, что распространенность поражения тканей пародонта в этой же возрастной группе — 82 % [6]. Актуальность связана не только с высокой распространенностью, но и омоложением данной патологии.
Несмотря на большое число исследований и имеющееся разнообразие схем, методов и средств комплексного лечения, проблема изучения новых технологий для терапии и профилактики этой патологии остается актуальной, так как распространенность ВЗП не уменьшается, приводя к появлению преждевременных дефектов зубного ряда, снижая трудоспособность и качество жизни, обладая системным воздействием на организм, способствуя развитию различных патологических процессов.
Сегодня дентальная имплантация является передовым методом лечения стоматологических заболеваний различной этиологии, связанных с потерей зубов [2].
Лавинообразно растет количество устанавливаемых стоматологами имплантатов, расширяются показания к имплантации, однако на фоне широкого внедрения дентальной имплантации в стоматологическую практику не уменьшается, а, по данным ряда авторов, увеличивается количество осложнений [1]. Несмотря на то что имплантация в последние годы отличается высоким уровнем успеха в раннем послеоперационном периоде, в научной литературе появляется все больше сведений о риске отдаленных осложнений.
Воспаление тканей, окружающих остеоинтегрированный имплантат, является одной из основных проблем имплантологии [3, 4]. В 2008 г. на рабочем совещании Европейской федерации пародонтологии на основе современной научной доказательной базы было выработано согласованное мнение об инфекционно-воспалительных поражениях в области дентальных имплантатов. Предложено выделять периимплантационный мукозит и периимплантит.
Мукозит в области имплантата — это воспаление окружающих мягких тканей без нарушения остеоинтеграции. Дентальный периимплантит — это воспалительная реакция тканей, окружающих остеоинтегрированный имплантат, сопровождающаяся потерей опорной кости [8]. Современные данные свидетельствуют о том, что мукозит может возникать у 80 % лиц, имеющих дентальные имплантаты, а развитие периимплантита описано у 28—56 % обследованных лиц [11].
Интенсивные эпидемиологические исследования заболеваний пародонта привели к существенным изменениям общей концепции этиологии и патогенеза и предопределили новые приоритеты в диагностике и лечении данной патологии [9].
Современный уровень знаний патогенеза пародонтита и периимплантита определяет воспалительную концепцию в качестве основной как результат взаимодействия микроорганизм — хозяин. В ответ на бактериальную агрессию возникает стереотипная воспалительная реакция, которая создает предпосылки для формирования воспалительного инфильтрата, способного вызвать вторичную альтерацию тканей пародонта вследствие чрезмерного действия цитокинов [5].
Сегодня дентальная имплантация является передовым методом лечения стоматологических заболеваний различной этиологии, связанных с потерей зубов
Хроническое течение ВЗП предопределяет формирование биопленки — сообщества микроорганизмов, взаимодействующих между собой и защищенных синтезированной ими экзополисахаридной оболочкой, не дающей антисептикам, противомикробным средствам и антибиотикам взаимодействовать с рецепторами бактериальных мембран, таким образом, делая их недоступными для проводимой местной и общей терапии, что значительно снижает эффективность и долгосрочность результатов лечения. Поэтому основной задачей лечения и профилактики ВЗП является своевременное удаление биопленки с поверхности твердых тканей зуба и из пародонтальных карманов [7].
Многочисленные научные обоснования ассоциативной бактериальной этиологии, сложного многоуровневого патогенеза воспалительных заболеваний пародонта инициировали внедрение в практику пародонтолога методов, позволяющих разрушить биопленку.
Метод Perio-Flow (EMS, Швейцария), основанный на воздушно-абразивной очистке пародонтальных (периимплантатных) карманов от биопленки порошком глицина (размером частиц 25 мкм), был внедрен в пародонтологическом подразделении хирургического отделения автономного учреждения здравоохранения «Республиканская стоматологическая поликлиника» в 2010 году.
Целью исследования явились оценка и обоснование клинической эффективности новой воздушно-абразивной технологии в комплексном лечении и профилактике воспалительных заболеваний пародонта и периимплантита по сравнению с традиционными методами.
Материалы и методы
Группу исследования сформировали из пациентов (92 человека), обратившихся в пародонтологический кабинет АУЗ «Республиканская стоматологическая поликлиника г. Уфы». Для статистической чистоты группа исследования с пародонтитом (75 человек) формировалась равномерно однородной по полу (50 % мужчин, 50 % женщин), возрасту (35—44 года), без выраженной соматической патологии и с неотягощенным аллергологическим анамнезом, одинаковой по клиническому статусу — диагноз у всех исследуемых: «хронический генерализованный пародонтит средней степени тяжести в стадии обострения (глубина пародонтальных карманов (ПК) до 5 мм, уровень резорбции костной ткани по ортопантомограмме не более 1/3—1/2 длины корня зуба), с отсутствием дефектов зубного ряда и значительных ортодонтических отклонений».
Возраст пациентов с воспалительным процессом в области имплантатов (17 человек) составил 24—56 лет, 9 мужчин и 8 женщин, срок пользования имплантатами — от 1 года до 7 лет, имплантаты как во фронтальных участках, так и в области премоляров и жевательных зубов (всего 24 имплантата). Диагноз «периимплататный мукозит» — у 2 пациентов, у остальных — периимплантит. Сопутствующим стоматологическим заболеванием у 6 из пациентов с имплантатами (35,29 %) был хронический генерализованный пародонтит в стадии обострения — легкой степени (ХГПЛС), у 11 (64,71 %) средней степени тяжести (ХГПСС).
В комплекс лечения всех пациентов включались мотивация и обучение гигиене полости рта (ГПР), профессиональная гигиена полости рта (ПГПР): зубные отложения (ЗО) снимали при помощи PIEZON® MASTER 700 (EMS, Швейцария), зубной налет (ЗН) очищали воздушно-абразивным аппаратом AIR-FLOW® MASTER (EMS) с использованием порошка AIR-FLOW® Classic (гидрокарбонат натрия, диаметр частиц 65 мкм) — в области имплантатов вручную неабразивными пастами, проводилась местная и (по показаниям) общая противомикробная и противовоспалительная терапия, физиотерапия (лазер), витаминотерапия, местная иммунокоррекция.
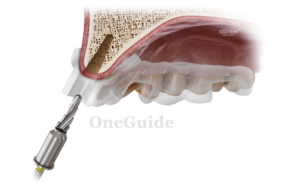
В основной группе, помимо стандартной ПГПР, проводилось снятие биопленки методом Perio-Flow (EMS) (воздушно-абразивная обработка порошком глицина диметром частиц 25 мкм) (рис. 1) на 2-й день (2-е посещение), через 6 недель (5-е посещение), через 3 месяца (6-е посещение).
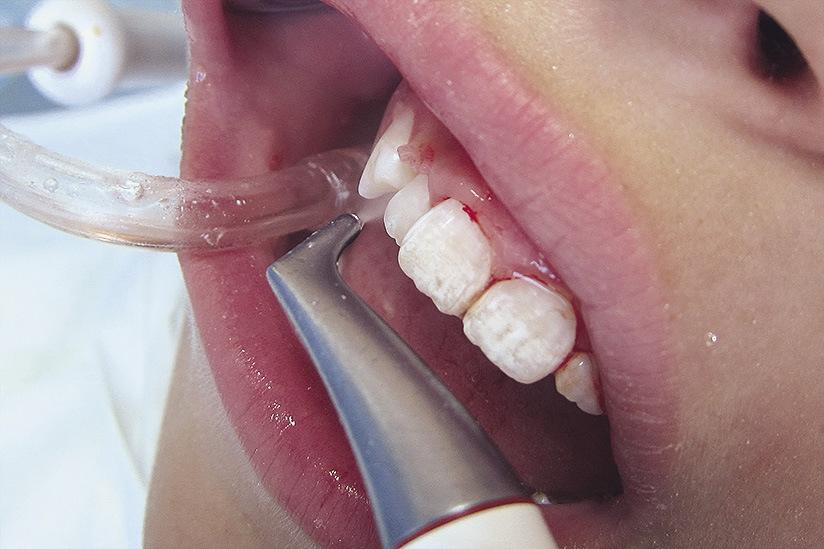
Рис. 1а. Обработка методом Perio-Flow пародонтального кармана глубиной до 3—4 мм (наконечником Air-Flow) и 5 мм (наконечником Perio-Flow с одноразовым пластиковым носиком Perio)
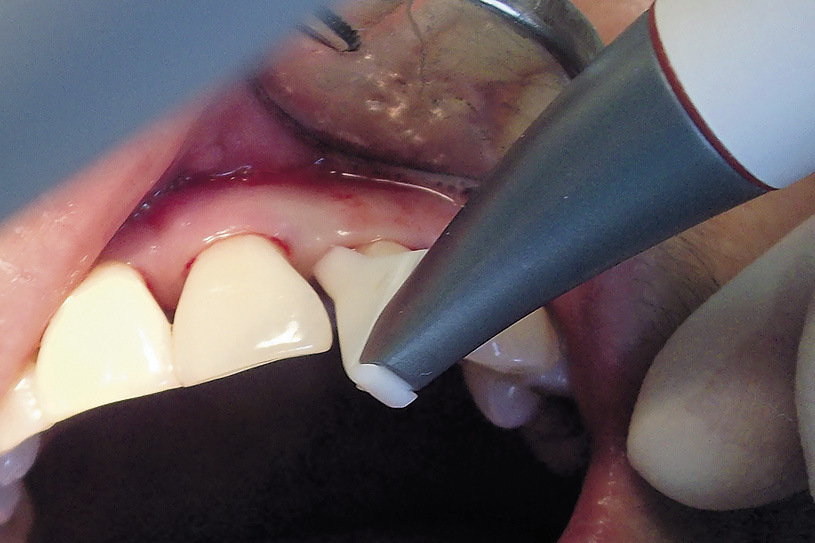
Рис. 1б. Обработка методом Perio-Flow пародонтального кармана глубиной до 3—4 мм (наконечником Air-Flow) и 5 мм (наконечником Perio-Flow с одноразовым пластиковым носиком Perio)
Критериями оценки эффективности лечения являлись результаты клинико-рентгенологических и инструментальных методов исследования, полученные на этапах наблюдений. Для анализа результатов проводимой терапии оценивали глубину пародонтального кармана (глубину зондирования вокруг имплантата — периимплантатный карман (ПИК), цвет периимплантатной десны, консиситенцию, наличие или отсутствие экссудата из периимплантатной бороздки (кармана), величину периимплантатной маргинальной костной резорбции, упрощенный индекс гигиены полости рта (ГПР) OHI-S (J. C. Green, J. K. Vermillion, 1963), индекс для количественного определения налета в придесневой области Silness-Loe (S-L) (Silness J., Loe, H., 1964), индекс кровоточивости PBI (papilla bleeding index) (Мuhllemann-Sukser), индекс PMA (papillar-marginal-alveolar) (I. Schour, M. Massler, 1947, в модификации С. Parma, 1960).
Для оценки состояния костной ткани проводили цифровую ортопантомографию на аппарате TROPHYPAN eXpert DC.
Оценка клинических параметров и индексная оценка проводилась в каждое из посещений пациента (на 1-й день, на 2-й день, на 5-й день, на 10-й день, через 6 недель, через 3 месяца, 6 месяцев) — всего 7 посещений. Анализ полученных данных производился с помощью стандартных статистических методов. Для всех критериев и тестов величина критического уровня значимости принималась равной 0,05, то есть различия признавались статистически значимыми при р<0,05. Полученные значения выражались в виде среднего значения и ошибки среднего значения (M±m). Сравнение средних показателей двух групп проводили с помощью критерия Стьюдента (t).
Результаты исследования
До лечения индексы гигиены и состояния десны оставляли желать лучшего в обеих группах. Глубина ПК, ПИК варьировала от 3,5 до 5,2 мм, индекс кровоточивости PBI в среднем составлял 4,1±0,1, индекс PMA — 52,6 ±3,9 %. Высокие показатели индекса гигиены полости рта Silness-Loe (2,86±0,05) и OHI-S (3,2±0,08) указывали на то, что практически у всех пациентов была неудовлетворительная гигиена полости рта.
У пациентов обеих групп во время лечения заметно улучшилось гигиеническое состояние полости рта, согласно уровню индекса OHI-S до нормы (удовлетворительная гигиена полости рта) — 0,8±0,03, который, незначительно увеличившись к последующим посещениям (до 0,97±0,04 и 1,05±0,04), оставался достаточно стабильным на протяжении всего срока наблюдения.
В результате исследования выявлены различия в степени редукции индекса придесневого налета Silness-Loe. Так, на 3-е посещение (через 6 недель) индекс S-L составил 0,5 ± 0,02 в основной группе и 0,9 ± 0,03 в контрольной, на 5-е (через 3 месяца) — 0,6 ± 0,03 и 1,1 ± 0,04 (p<0,01), и через 6 месяцев разница составляла почти 2 раза — 0,68 ± 0,03 в основной группе и 1,22 ± 0,04 в контрольной (p<0,01) (рис. 2).
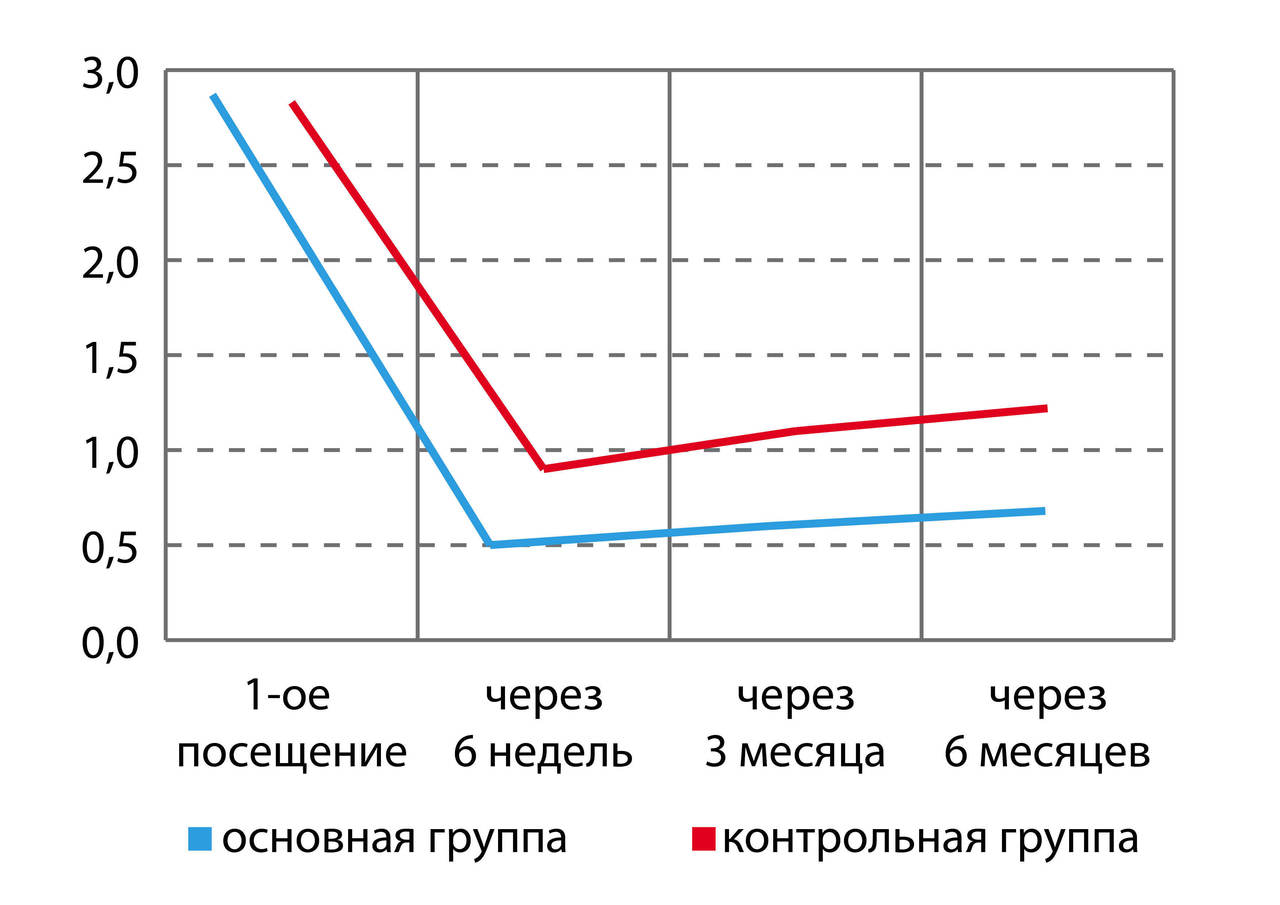
Рис. 2. Сравнительная характеристика динамики индекса придесневого налета Silness-Loe в основной и контрольной группах в течение срока наблюдения
Так как гигиена над десной (OHI-S) после лечения и коррекции гигиенических навыков одинаково удовлетворительная, разница в индексе придесневого налета S-L, по нашему мнению, может быть обусловлена результатом профессиональной гигиены, полноценное удаление поддесневого налета и биопленки Perio-FLOW позволяет устранить микронеровности и достичь максимальной гладкости поверхности, что в дальнейшем уменьшает риск образования зубного камня и ретенции зубного налета, а значит, снижается потенциальный риск воспаления.
Снижение выраженности воспалительных явлений (кровоточивости десен, исчезновение неприятного запаха изо рта, снижение или полное исчезновение болевых ощущений в деснах) происходило в основной группе по сравнению с контрольной более высокими темпами — на 15,3 ± 3,4 % больше редукция PBI в 3-е посещение и на 10,2 ± 3,7 % в 4-е (p<0,05). Удаление биопленки позволило быстрее снизить явления отечности десны, гиперемию, отделяемое из ПК. Изменение уровня индекса PMA также показало большую эффективность в снятии клинических симптомов воспаления метода лечения с включением в комплекс метода Perio-Flow.
Динамика изменения глубины пародонтального (периимплантатного) кармана в процессе проводимых наблюдений значительно различалась в основной и контрольной группах.
Через 6 недель после начала лечения редукция глубины пародонтального кармана в основной группе составила 15,5±1,2 %, через 3 месяца — 18,4±1,4 %, через 6 месяцев — 18,9±1,5 %, в контрольной же группе уровень редукции максимально достиг уровня 7,9±1,2 % к 3-му месяцу от начала лечения (p<0,01) с незначительным снижением через 6 месяцев.
Заключение
Полученные во время клинических наблюдений и исследований сравнительные оценки результатов традиционных и современного методов профессиональной гигиены позволили сделать выводы о превосходстве последнего по всем параметрам. Результативность лечения в основной группе объясняется активным воздействием на главный этиологический фактор — биопленку, что является основой длительности поддержания должного уровня индекса гигиены, а следовательно, клинических параметров ремиссии. Уменьшение глубины пародонтальных (периимплататных) карманов обусловлено восстановлением биосовместимости тканей пародонта в процессе процедуры Perio-Flow за счет биомодификации воздушно-порошковой смесью глицина.
Объективные данные гигиенических, пародонтальных индексов и клинических показателей процессов заживления в ранние (до 6 недель) и отдаленные (до 6 месяцев) сроки наблюдения подтвердили высокую клиническую эффективность включения в комплекс профессиональной гигиены при лечении периимплантита и пародонтита современной малоинвазивной технологии для удаления биопленки PERIO-FLOW. Результаты исследования являются обоснованием для рекомендации применения этой технологии в стоматологической практике в качестве эффективного средства профессиональной гигиены во время комплексного лечения и для профилактики воспалительных заболеваний пародонта и периимплантита.
- Ахмадова М. А., Игнатов А. Ю. Дентальная имплантация с применением навигационного имплантологического шаблона, изготовленного по технологии CAD/CAM // Стоматология. — 2011, № 2. — С. 49—52.
- Кулаков А. А., Буцан С. Б., Сухарский И. И. и др. Планирование и проведение этапа дентальной имплантации на основании компьютерного моделирования в сложных клинических ситуациях // Стоматология. — 2011, № 2. — С. 38—42.
- Соловьева А. М. Периимплантит: этапы достижения консенсуса в диагностике и лечении // Клиническая стоматология. — 2010, № 4. — С. 50—52.
- Тлустенко В. П., Гильмиярова Ф. Н., Головина Е. С. и др. Доклиническая диагностика дентального периимплантита // Российский стоматологический журнал. — 2011, № 2. — С. 28—29.
- Черкашин Д. С., Григорович Э. Ш., Городилов Р. В. Оценка эффективности консервативного лечения больных хроническим генерализованным пародонтитом // Институт стоматологии. — 2009, № 1. — С. 68—69.
- Янушевич О. О., Кузьмина И. Н. Состояние тканей пародонта у населения в возрасте 35—44 лет в регионах России // Российский стоматологический журнал. — 2009, № 1. — С. 40—41.
- Herbert F. Wolf, Edith M. & Klaus H. Rateitschak Пародонтология (перевод с нем. под ред. Барера Г. М.). — М., 2008. — 548 с.
- Lindhe J Meyle J. Group D of European Workshop on Peri-odontology. Pen-implant diseases: Consensus Report of the Sixth European Workshop on Periodontology. — J Clin Periodontol. — 2008; 35 (8 Suppl): 282—285.
- Shay K. Oral infections in the Elderly. — Part I: Bacterial infections of the mouth // Clinical Geriatrics. — 2006. — V. 14. — P. 36—45.
- WHO-EURO. Health for all, List of Statistical Indicators. — Copengagen, World Health Organization; Regional Office for Europe. — 1994. — 131 p.
- Zitzmann N. U., Berglundh T. Definition and prevalence of pen-implant diseases. — J Clin Periodontol. — 2008; 35 (8 Suppl): 286—291.