Использование бифазного остеокондуктивного замещающего кость материала EasyGraft® Crystal при замещении костных дефектов
А. В. Павленко
профессор, директор Института стоматологи Национальной медицинской академии последипломного образования им. П. Л. Шупика
Г. Б. Проць
доцент кафедры хирургической стоматологии Ивано-Франковского государственного национального медицинского университета
А. Б. Баранов
врач стоматолог-ортопед (Краснодар)
А. Х. Штеренберг
к. м. н., B.Sc. Ph.D., лектор-консультант компании Sunstar Guidor (Zurich, Switzerland)
Сохранение костной ткани, создание адекватного объема и регенерация кости — по-прежнему самые актуальные темы хирургической стоматологии, имплантологии и пародонтологии. Для того чтобы осуществить все эти мероприятия, используется огромное разнообразие различных костных и замещающих кость материалов. Однако все больше и больше появляется в литературе публикаций, указывающих на то, что очень много врачей-имплантологов перестали увлекаться собственной костью пациента как материалом для восстановления утраченной костной ткани для имплантологических целей.
Забор собственной кости у пациента — это всегда вторая операция, которая небезразлична пациенту. Через полгода при раскрытии прооперированной области, как правило, остается половина подложенного материала. Мы не будем в данной статье повторяться в рассказах обо всех применяемых сегодня в стоматологии остеотропных материалах.
Хотим обратим ваше внимание на то, что в последние годы все большую популярность приобретают материалы синтетического происхождения. Особенно материалы, которые имеют такие свойства, как технологичность, биосовместимость, высокая пористость, резорбируемость, способность выступать в роли матрицы при регенерации костной ткани. Чтобы быть уверенным, что предполагаемое лечение будет как можно менее травматичным, все чаще и чаще стали применяться замещающие кость материалы на основе ?-ТКФ, такие как easy-graft® и easy-graft® CRYSTAL.
Основное назначение замещающих кость материалов — выступать в роли платформы. Они способствуют регенерации костной ткани, которая начинается от костной стенки дефекта и распространяется через материал к центру дефекта (Lu Z et al. 2010). Человеческая костная ткань в большей части своего неорганического состава содержит (около 70 %) модифицированный гидроксиапатит, который состоит, прежде всего, из Ca? (кальций) и PO? (фосфат).
Использование синтетических фосфатов кальция как заменителей кости рассматривалось очень давно из-за химической композиции, подобной структуре костной ткани. Первый документ клинического применения кальцийфосфатных соединений датирован 1920 г. Фосфаты кальция использовались как замещающие кость материалы в хирургической стоматологии почти до конца 1970 года (Le Geros et al. 2003).
Сегодня синтетические кальцийфосфаты очень широко применяются, как замещающие кость материалы, для заполнения различных костных дефектов в повседневной клинической практике.
Чаще всего применяются такие варианты:
- Монофазный замещающий кость материал ?-трикальцийфосфат (?-ТКФ; Ca3(PO4)2.
- Гидроксиапатиты: НА Ca10(PO4)6(OH)2.
- Бифазный кальцийфосфат БКФ, представляющий соединение ?-ТКФ и НА.
Все три материала в большинстве своем содержат кальций и фосфат в различных пропорциях.
?-TКФ, HA и БКФ отличаются друг от друга только степенью резорбции, где самый высокий уровень принадлежит ?-TКФ, а самый низкий — НА. Однако резорбируемость материала не зависит исключительно от типа кальцийфосфата. Многие другие факторы, такие как пористость, технологичность, влияют на уровень резорбции.
Easy-graft® содержит чистую фазу ?-TКФ и подтвержден как монофазный материал, полностью резорбируемый в течение нескольких месяцев (Nair et al. 2006; Rothamel et al. 2007; Glaser 2009).
Easy-graft® — это бифазный материал и состоит из 60 % НА и 40 % ?-TКФ. Он резорбируется частично и сохраняет НА, окруженный вновь сформированной костной тканью, на более длительный период.
Пористость замещающего кость материала является ключевым фактором в регенерации костной ткани.
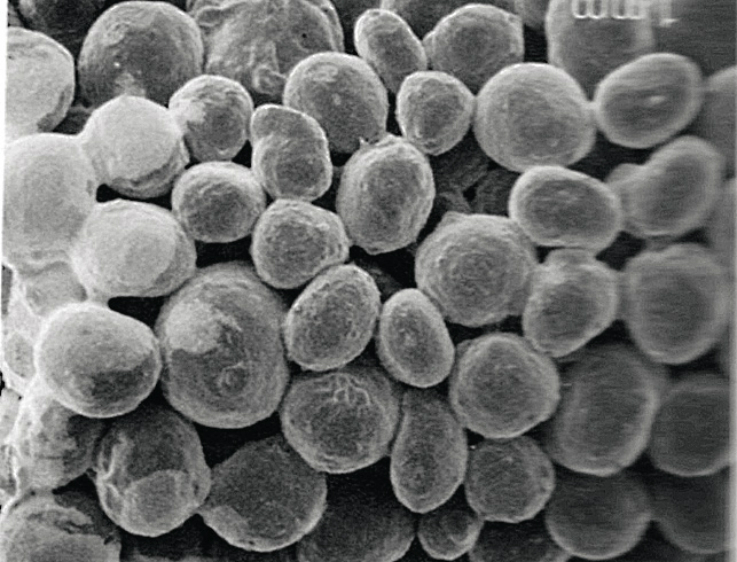
Макропористость материала — это наличие пространства между круглыми, устойчивыми к давлению гранулами, что создает благоприятные условия для формирования новой кости, и развитию ангиогенеза, необходимого для обеспечения питания новых тканей и выведения продуктов метаболизма. Однако следует помнить, что гранулы должны быть достаточно прочными, чтобы во время применения этих материалов не наступала их фрагментация или раскалывание (рис. 1).
Высокая микропористость кальцийфосфатов (размер пор от 1 до 10µм) увеличивает остеокондуктивные свойства материала, а также увеличивает регенерацию новой кости по сравнению с материалами, не обладающими микропористостью (Habibovic et al. 2005: Hing et al. 2005; Habibovic et al. 2006).
Общеизвестный факт, что поры являются своеобразными нишами для остеогенных клеток, поэтому материалы с открытыми пористыми системами очень привлекательны для факторов роста. Особенно таких важных для регенерации костной ткани факторов, как PDGF-факторы, стимулирующие остеобласты, и VTGF-факторы, стимулирующие образование эндотелия сосудов. Вновь сформированная костная ткань, обнаруженная в микропорах, подтверждает тот факт, что процесс интеграции кальцийфосфата происходит на микропористом уровне (Lan Levengood et al. 2010). Еasy-graft® CRYSTAL — открытая микропористая структура.
В этой статье мы расскажем о втором поколении остеотропных материалов на основе ?-трикальцийфосфата того же производителя. Это материал Еasy-graft® CRYSTAL.
Easy-graft® CRYSTAL состоит из бифазного кальцийфосфата БКФ в композиции 60 % искусственного гидроксиапатита и 40 % ?-ТКФ.
При производстве easy-graft® CRYSTAL не просто производится смешивание двух материалов, а создается истинное новое соединение НА и ?-ТКФ. Это означает, что каждая гранула материала easy-graft® CRYSTAL состоит из двух материалов (рис. 2).
Бифазный кальцийфосфат пришел в хирургическую стоматологию из ортопедии (Passuti et al. 1989; Delecrin et al. 2000; Xie et al. 2006). Он используется при операции синус-лифта с одномоментной установкой имплантатов (Cordaro et al. 2008; Froum et al. 2008; Lee et al. 2008), при заполнении костных карманов (Sculean et al. 2008), при дефектах после удаления кисты (Piattelli et al. 1996), для заполнения лунки удаленного корня зуба (Weiss et al. 2007).
Как ведет себя easy-graft® CRYSTAL в организме?
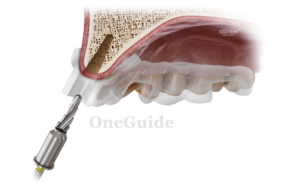
Входящий в состав бифазного материала ?-ТКФ (40 %) полностью резорбируется путем растворения в межтканевой жидкости, не последнюю роль играет и клеточный механизм (Lan Evengood et al 2010). Искусственный гидроксиапатит (60 %) остается в дефекте на более долгое время и продолжает выполнять роль остеокондуктивной матрицы. Это может быть рассмотрено как преимущество данной методики, особенно при больших дефектах (например, киста), как процесс замедленной регенерации. Конечный результат процесса заживления — это соединение новой собственной кости и НА. Интегрированный НА может обеспечивать профилактику атрофии и сохранять объем твердых тканей более длительное время (Zafiropoulos et al. 2007) (рис. 3—6).
- Рис. 3. Easy-graft® CRYSTAL при контакте с кровью твердеет.
- Рис. 4. Резорбируется оболочка ПЛГК.
- Рис. 5. Начинает резорбироваться ?-ТКФ.
- Рис. 6. НА замурован во вновь сформированную кость.
Клинический случай
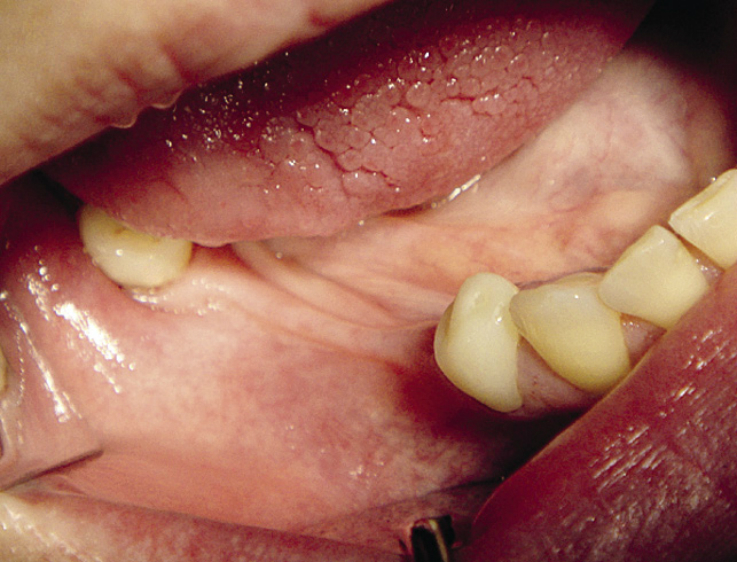
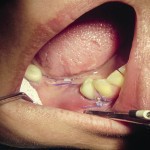
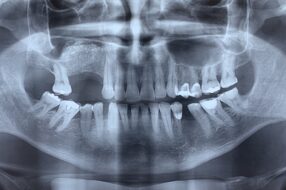
Применение материала easy-graft® CRYSTAL при узком гребне альвеолярного отростка в боковом отделе нижней челюсти: реабилитация стоматологических больных методом дентальной имплантации при узком гребне альвеолярного отростка нижней челюсти — довольно частая проблема дентальной имплантации (рис. 7).
Много различных хирургических методик по увеличению объема костной ткани атрофированного отростка нижней челюсти описано в литературе. Предлагаемые стратегии решения этой проблемы включают в себя использование блоков собственной кости, применение методики направленной костной регенерации, расщепление альвеолярного отростка и дистракционный остеогенез.
Технология расширения или расщепления узкого гребня альвеолярного отростка нижней челюсти сводится к созданию ложа под имплантаты путем горизонтального рассечения альвеолярной кости по центру отростка и создания двух послабляющих вертикальных рассечений для перемещения вестибулярной кортикальной пластинки в щечную сторону. Пространство между вестибулярной и язычной кортикальными пластинками, а также между имплантатами заполняется остеотропным материалом.
Данная методика всегда предусматривает одновременную установку имплантатов и в значительной степени сокращает сроки лечения пациентов. В представленном исследовании демонстрируется клиническое использование материала easy-graft® CRYSTAL для заполнения костного дефекта после расщепления узкого альвеолярного отростка нижней челюсти с одновременной установкой имплантатов.
После проведения местной инфильтрационной анестезии Sol.Septanest с эпинефрином 1/100 000 — 1,7 ml был произведен разрез мягких тканей по центру альвеолярного отростка. Длина горизонтального разреза зависит от количества устанавливаемых имплантатов и расстояния между имплантатами. Были также произведены два вертикальных разреза по вестибулярной поверхности альвеолярного отростка. Был отслоен полный слизисто-надкостничный лоскут, открывающий вестибулярную стенку отростка. С язычной стороны лоскут несколько смещался в сторону полости рта и целиком не откидывался для обеспечения хорошего кровоснабжения кости и сохранения его прикрепления.
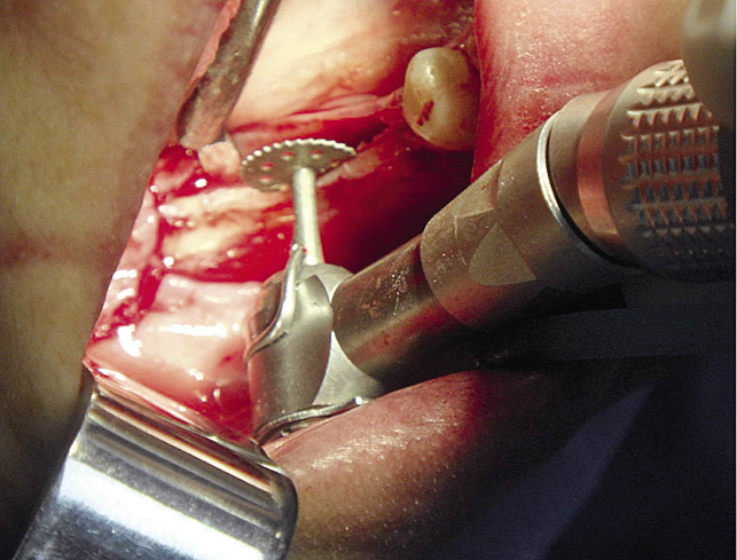
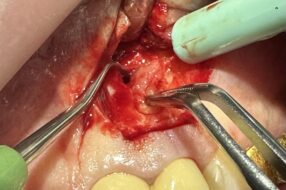
Горизонтальная кортикотомия производилась с помощью циркулярной пилы из набора инструментов для расщепления альвеолярного отростка немецкой компании Meisinger и начиналась с отступом 1—2 мм от зуба, ограничивающего дефект зубного ряда (рис. 8).
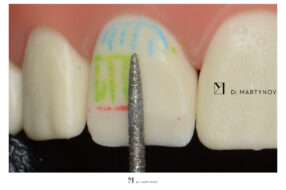
Два послабляющих вертикальных распила вестибулярной кортикальной пластинки осуществлялись с помощью алмазного конусовидного бора. Длина проведенных распилов была равна примерно половине длины предполагаемых для установки имплантатов. Однако глубина распилов осуществлялась на всю высоту кортикальной пластики.
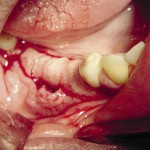
Перемещение вестибулярной кортикальной пластинки проводилось с помощью дистракторов и спредеров из этого же набора инструментов (рис. 9).
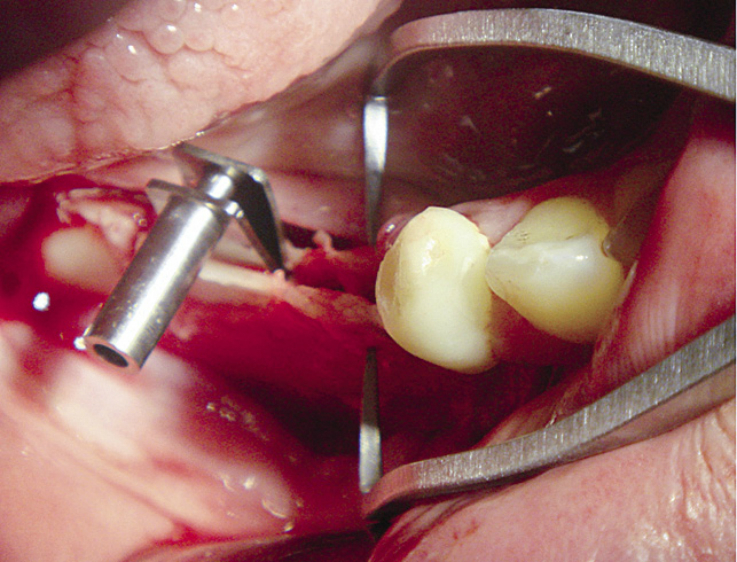
После создания финишным сверлом ложа имплантаты были установлены (рис. 10, 11).
- Рис. 10. Обозначение места установки имплантатов.
- Рис. 11. Установлены имплантаты.
После снятия дистракторов промежуток между пластинками и имплантатами был заполнен материалом easy-graft® CRYSTAL (рис. 12—15).
- Рис. 12. PRGF и мембрана.
- Рис. 13. Забор порции плазмы.
- Рис. 14. Фибриновая мембрана.
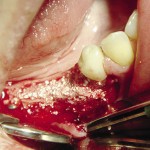
- Рис. 15. Дефект заполнен материалом easy-graft® CRYSTAL.
При контакте с кровью материал твердел и хорошо удерживался в дефекте. Слизисто-надкостничный лоскут был уложен на свое место и рана ушита нерассасывающимся шовным материалом (рис. 16—18).
- Рис. 16. Мембрана уложена на раневую поверхность.
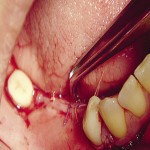
- Рис. 17. Рана ушита.
- Рис. 18. На 10-й день после операции.
Заключение
В настоящем исследовании при выполнении операции по расщеплению альвеолярного отростка нижней челюсти в качестве наполнителя промежутка между кортикальными пластинками и между имплантатами использовался бифазный материал easy-graft® CRYSTAL. Твердеющий в дефекте материал обеспечивал стабильность вестибулярной кортикальной пластинки и кровяного сгустка. Чем больше размер дефекта, тем больший объем кости должен быть сформирован и, соответственно, требуется больше времени на процесс заживления.
Материал easy-graft® CRYSTAL показан для использования при больших дефектах по двум соображениям. Первое: материал обладает высокой остеокондуктивностью, которая способствует формированию костных мостиков в дефекте. Второе: гидроксиапатит в данной композиции выступает как остеокондуктивная платформа, даже при увеличивающемся процессе заживления и регенерации. В данном клиническом случае материал easy-graft® CRYSTAL укладывался в виде «Наполеона», то есть послойно, с плазмой, богатой факторами роста. Для этой цели из собственной крови больного была получена плазма, богатая факторами роста (PRGF), и фибриновая мембрана, которая была уложена поверх материала и имплантатов.
Cписок литературы находится в редакции
Статья была опубликована в журнале «Современная Стоматология» № 1, 2013, стр. 89—92, Национальной медицинской академии последипломного образования (Киев, Украина).