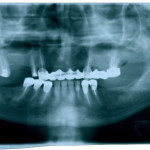
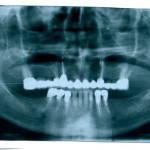
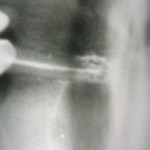
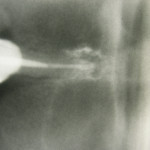
Лечение пародонтоза с использованием имплантационной системы на основе наноструктурированных интеллектуальных материалов и наногелей
Пародонтоз, т. е. дистрофически-дегенеративный процесс, распространяющийся на все структуры пародонта, чрезвычайно широко распространен среди взрослого населения. Изменения, развивающиеся в костной ткани пародонта под влиянием длительной нагрузки, перегрузки, перманентных однообразных повышенных нагрузок или, наоборот, в отсутствие адекватных нагрузок при адентии, ведут к развитию параморбидных адаптационных синдромов (ПАС) со срывом адаптационно-компенсаторных механизмов и переходом ПАС в болезнь [20].
Цель исследования
Разработка новых методов лечения пародонтоза при наличии адентии, пародонтита и деструктивных периодонтитов с использованием комплексной функциональной имплантационной системы на основе новых наноструктурированных интеллектуальных материалов и наногелей.
Материалы и методы
Гидроксиапатита наногель (ГАНГ) — остеопластический материал, наноструктурированный никелид титана (НСНТ) — материал для изготовления имплантатов с памятью формы и (в дисперсном состоянии) имплантат для замещения дефектов костной ткани, БоТП — богатая тромбоцитами плазма (аутокрови), ИМ — интерметаллид, ДИ — дентальная имплантация, ЭЭИ — эндодонто-эндоссальная имплантация, ИПД — интенсивная пластическая деформация, РКУП — равноканальное угловое прессование (никелида титана), СВС — самораспространяющийся высокотемпературный синтез (никелида титана), УЗМ — ультразвуковое микширование, ЭПФ — эффект памяти формы, НТ — нанотехнологии.
Лечение проводилось эндодонтическим и инъекционными — внутридесневым и внутрикостным методами введения материалов, а также методами ЭЭИ и ДИ имплантатами с эффектом памяти формы (ЭПФ).
Результатами проведенного лечения являются функционирование вылеченных зубов в течение более чем 4 лет по завершении лечения деструктивных (со значительной степенью деструкции) периодонтитов причинных зубов эндодонтическим и инъекционно-внутрикостным методами или их комбинацией с ЭЭИ; увеличение объема костной ткани челюсти (с уплотнением ее структуры) инъекционно-внутрикостным методом, восстановление целостности зубных рядов ДИ в комбинации с гетерофазными композитами на основе БоТП при адентии.
Предпосылки создания системы
Пародонтоз, т. е. дистрофически-дегенеративный процесс, распространяющийся на все структуры пародонта, чрезвычайно широко распространен среди взрослого населения. Изменения, развивающиеся в костной ткани пародонта под влиянием длительной нагрузки, перегрузки, перманентных однообразных повышенных нагрузок или, наоборот, в отсутствие адекватных нагрузок при адентии, ведут к развитию параморбидных адаптационных синдромов (ПАС) со срывом адаптационно-компенсаторных механизмов и переходом ПАС в болезнь [20]. Прогрессирование процесса ведет к атрофии тканей пародонта (прежде всего, костной), а ослабление общих и местных защитных механизмов ведет к развитию явлений воспалительной деструкции пародонта [3]. Соответственно, лечение пародонтоза должно быть комплексным и по возможности щадящим.
Однако на сегодняшний день комплексного малотравматичного метода лечения пародонтоза с одновременным лечением воспалительных заболеваний пародонта не существует [5]. В связи с этим возникает необходимость в поиске принципиально новых подходов к решению этой актуальной и социально значимой задачи. Цель настоящей работы — предложить комплексную имплантационную систему для лечения пародонтоза и сопутствующих ему пародонтитов, периодонтитов и адентии.
Теоретическое обоснование применения системы
Теоретическим обоснованием применения системы является закон, сформулированный Wolff J. (1872), о том, что в основе каждой регенерации лежит стремление природы восстановить не форму, а функцию. Roux W. (1893), в свою очередь, обосновал, что кость имеет функциональные форму и строение и происходит это оттого, что функциональное раздражение вызывает трофическое раздражение клеток, в результате чего увеличивается питание кости, увеличение питания ведет и к увеличению кости, уменьшение, наоборот, ведет к ее атрофии.
Л. П. Соковым (2002) обосновано учение о параморбидных адаптационных синдромах в продолжение учения Г. Селье об адаптационном синдроме [18].
Элементы системы и их применение
Предлагаемая система представляет собой комплекс наноструктурированных материалов, имплантатов и устройств, а также методы лечения с их применением. Смысл применения этой системы в том, что она позволяет не удалять подвижные зубы и корни зубов со значительной деструкцией периодонта, а восстанавливать их, одновременно восстанавливая то, что у пациента утрачено или разрушается, а именно костную ткань челюсти, соединительную ткань десны и периодонт зубных корней.
Основными элементами системы являются разработанный совместно инновационным стоматологическим центром «НАНОДЕНТ» и Электростальским политехническим институтом композиционный материал на основе наноструктурированного никелида титана (НСНТ) — «неживая составляющая» и богатая тромбоцитами плазма (БоТП) крови пациента — «живая составляющая», которые после ультразвукового микширования в виде геля инъекционно вводятся в ткань.
Также система представлена ЭЭИ с памятью формы, применяемыми для восстановления и протезирования корней зубов, типовыми ДИ с памятью формы, устройствами для остеосинтеза, инъекторами для инъекционного введения биокомпозитов на основе аутоплазмы крови как в комбинации с имплантатами, так и самостоятельно в зависимости от клинической картины.
Изменения, развивающиеся в костной ткани пародонта под влиянием длительной нагрузки, перегрузки, перманентных однообразных повышенных нагрузок или, наоборот, в отсутствие адекватных нагрузок при адентии, ведут к развитию параморбидных адаптационных синдромов
Традиционно применяемые стандартные дентальные имплантаты не позволяют получить полного соответствия имплантата и окружающей его ткани утерянному зубу по двум причинам: все временя присутствия имплантата в теле он остается неизменным, а окружающая его ткань деформируется под нагрузкой, растет, отмирает, то есть изменяется. При этом точное воспроизведение имплантатом анатомо-физиологических параметров функционировавшего ранее в челюстной кости корня зуба невозможно, поскольку имплантат вводится в высверленное врачом в челюстной кости имплантационное ложе, которое в этот момент представляет собой зияющую рану с поврежденной поверхностью, лишенную периодонта. Периодонт же, т. е. соединительнотканная связка, окружающая корень зуба, — главный инструмент сохранения корня зуба даже при полном разрушении коронки.
Эти факторы в основном, кроме еще ряда других, определяют ограниченный срок присутствия имплантата в организме. А ведь имплантат должен существовать в организме пожизненно, независимо от возраста больного. При этом имплантат должен полностью повторять характерную для живой ткани реакцию на нагрузку — по мере перемещения под нагрузкой, например при жевании, должно возрастать пристеночное сопротивление. Кроме того, интегрированная в кость часть имплантата на границе имплантат — кость вместе с контактирующей с имплантатом костной тканью должны выполнять демпферную функцию, присущую утраченному вместе с корнем зуба периодонту, и образовать со временем некий буфер, способный изменяться в соответствии с возрастным изменением окружающих тканей.
Принятая сегодня за основу непосредственная остеоинтеграция оправдывает себя в тех случаях, когда имплантат интегрирован в плотную мелкоячеистую губчатую челюстную кость с выраженным компактным слоем. В то же время не следует ожидать выраженной первичной стабильности имплантата в крупноячеистой губчатой кости с тонкой кортикальной пластинкой [4]. Если соединение имплантат — костная ткань будет неподвижным, это может привести к его отторжению [24].
Методы наноструктурирования, улучшающие физико-механические свойства никелида титана, также улучшают его биофункционалные свойства, оптимизируя интеграцию имплантатов с костной тканью
Живая ткань организма всегда фрактальна, т. е. структурные единицы ткани в наименьшем ее объеме имеют максимально допустимые численность и взаимосвязи, при которых каждая структурная единица ткани в отдельности выполняет ту же функцию, что и сама ткань. При этом репаративно-регенеративные процессы в ткани происходят путем самоорганизации, путем создания функциональной структуры, характерной именно для данного участка ткани, с учетом локальных функциональных изменений органотипа. Современные технологии позволяют получать материалы со специфическими функциональными характеристиками на молекулярном уровне (интеллектуальные материалы [21].
Примером интеллектуального материала является ИМ никелид титана с ЭПФ. ИПД (РКУП сплава ИМ и размол частиц ИМ на закритической скорости) сегодня позволяют наноструктурировать ИМ никелид титана и существенным образом улучшить его эксплуатационные свойства в заданном направлении, в первую очередь, как медицинского материала нового поколения [7].
Технически это выражается в повышении коэффициента деформационного упрочнения, пределов дислокационной текучести и прочности и т. д. Наряду с этим методы наноструктурирования, улучшающие физико-механические свойства никелида титана, также улучшают его биофункционалные свойства, оптимизируя интеграцию имплантатов с костной тканью.
НСНТ, синтезированный путем диффузионного насыщения никеля титаном с последующим размолом частиц ИМ до наномикроразмерного диапазона [1] и образования путем УЗМ полученных частиц НСНТ с микрочастицами механически фрагментированной БоТП, в комбинации с имплантатами, изготовленными из наноструктурированного ИПД РКУП сплава никелида титана, имеет повышенную по сравнению с обычным титаном биосовместимость, что в эксперименте проявляется ускоренным ростом клеток на поверхности такого гетерофазного имплантата в сравнении с контрольной титановой подложкой [2].
Нанотехнологии, т. о., позволяют получать биосовместимые фрактально организованные материалы, что позволяет приблизиться к решению задачи создания функциональной структуры, способной выполнять вокруг имплантата те же функции, что и периодонт — вокруг зубного корня. Решение этой задачи следует искать в создании компаундов из материалов живой и неживой природы, обладающих функциями самоорганизации и самосборки [22].
Самосборка подразумевает, что состав такого материала определяется свойствами окружающей имплантат среды и меняется от точки к точке. Функцию самосборки должна обеспечить «неживая», металлическая составляющая имплантата.
Самоорганизация определяет форму и свойства буферной связки на границе имплантат — кость в зависимости от изменения формы, окружающей ткани, и изменения характера внешней нагрузки. Эту функцию должна обеспечить «живая» составляющая имплантата.
Основу этого компаунда составляет наноструктурированный никелид титана, синтезированный путем диффузионного насыщения никеля титаном с «подавлением» СВС интерметаллида [10]. Интерметаллическое соединение титана с никелем образуется без повышения температуры при реакции. Образующийся продукт имеет минимальные температурные искажения кристаллической решетки. Такой никелид титана имеет стехиометрический состав, все образующие его атомы титана и никеля связаны, и поэтому он нетоксичен, обладает сверхпластичностью и низкотемпературной памятью формы.
После синтеза частицы никелида титана деформируют для образования пластинчатой структуры и появления разрывов между кристаллическими плоскостями, как это показано на рисунке 1 [1].
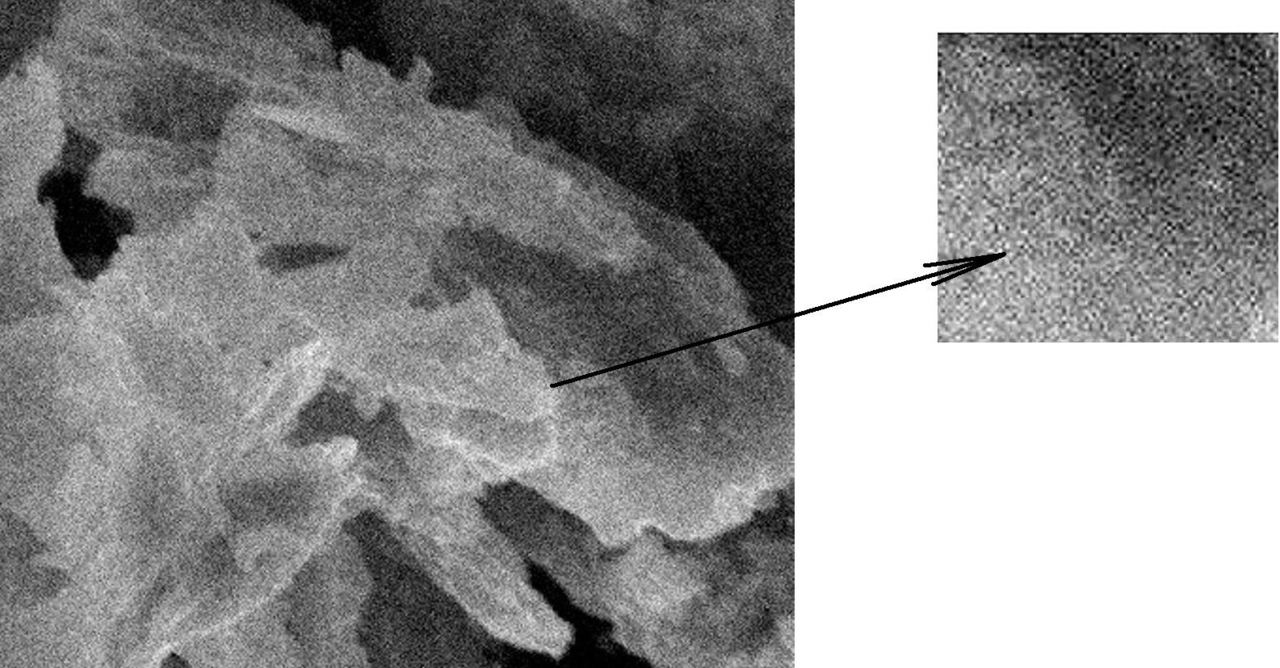
Рис. 1. Структура наночастиц никелида титана после размола на закритической скорости. Видна вытянутая форма кристаллитов и изрезанная, фрагментированная, фрактальная структура поверхности (фото лаборатории М-30, публикуется впервые).
Такая структура материала позволяет органической, соединительной или костной ткани интегрировать с частицами материала, которые становятся, таким образом, составной, органично вплетенной в ткань ее частью.
В состав компаунда входит ГАНГ — отечественный препарат производства фирмы «Медкам» (Москва) — биоактивный костнопластический материал на основе гидроксиапатита, имеющего кристаллически-аморфно-скрытокристаллическую структуру, с размерностью частиц 30—50 нм в гидратных оболочках и концентрацией гидроксиаппатита до 60 %, представляющий собой однородную гелевую композицию [13]. ГАНГ вводится в компаунд для повышения его функциональности в контакте с костной тканью, т. к. аморфно-скрытокристаллическая структура ГАНГ, с размерностью частиц гидроксиапатита 30—50 нм, позволяет молекулам гидроксиапатита напрямую встраиваться в костную ткань реципиента, минуя фазу рекристаллизации [12].
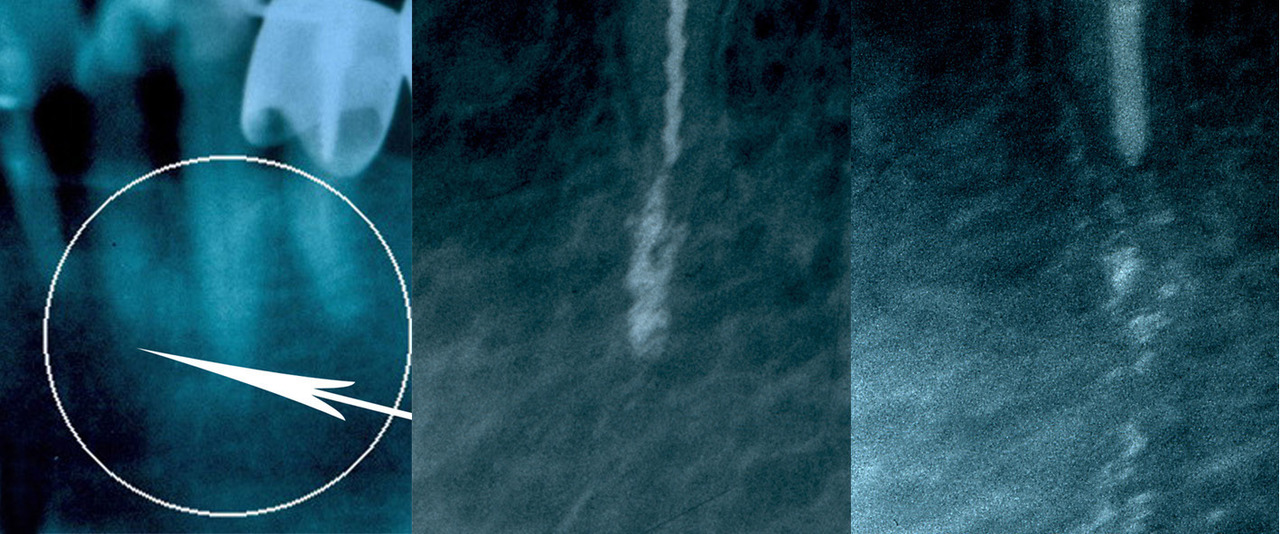
Рис. 2. 2.1 — прикорневой очаг разрежения костной ткани; 2.2 — введенный в прикорневую зону разрежения компаунд из наноструктурированного порошка никелида титана и ГАНГ, определяется в виде конгломерата; 2.3 — через 70 дней после лечения наночастицы никелида титана собрались в гранулы, участвуя в ремоделировании кости.
Для интенсификации процесса прорастания частиц никелида титана и снижения уровня бактериальной и грибковой опасности в компаунд добавляют коллоидные частица серебра [11].
Биологические эксперименты с применением наноматериалов доказали, что синергетика (самоорганизация) структур присуща как живым объектам, так и неживым и что структуры, формируемые нанообъектами, являются, прежде всего, функциональными [17].
Неорганические наночастицы в таких вновь организуемых биокомпозитах локализуются именно в тех пограничных участках на границе раздела фаз гетерофазного биокомпозита, где больше всего вакансий и, следовательно, наночастицы являются модификаторами функционального биокомпозита.
Модифицирующая способность наночастиц базируется на их большом энергетическом потенциале — суммарная энтальпия наночастиц гидроксиапатита кальция достигает 10 квт*час/кг, что на огромной (до 600 м2/грамм) удельной поверхности позволяет при их ничтожной концентрации (0,01—0,1%) перекрыть всю площадь границ раздела фаз композита [23].
С другой стороны, высокая поверхностная энергия наночастиц приводит к их мощному взаимодействию [22]. Дезинтеграцию частиц гидроксиапатита кальция, наночастиц никелида титана и мицелл серебра осуществляют в плазме крови (БоТП) посредством УЗМ.
Образуется устойчивая ультратонкая суспензия взвешенных наночастиц в олигопептидных связующих, при отсутствии механодеструкции [12].
Наноникелид титана — серебряный композит (НАНОНТС), подготовленный к применению, представляет собой нанокомпозиционный жидкотекучий гель, который шприцем вводят в костную ткань, проводя инъекционную остеопластику, или в имплантационное ложе непосредственно перед установкой ДИ или ЭЭИ [14].
Изменения состояния соединительной и костной тканей передаются органично вплетенным в их состав наночастицам никелида титана, объединяющимся вначале в гранулы, а затем в пористое тело, интегрирующее с тканью. В дальнейшем образуется прочный каркас с возможностью деформирования и изменения размеров в соответствии с приложенной нагрузкой.
Взаимодействие компаунда «НАНОНТС» с костной тканью
Установлено, что микро- и наночастицы никелида титана выполняют каркасообразующую функцию для трабекул костной ткани с образованием композита «НАНОНТС-кость» [7].
Взаимодействие компаунда «НАНОНТС» с периодонтом зубов
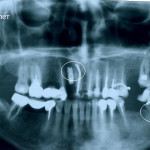
Установлено, что наночастицы никелида титана интегрируют с периодонтом вылеченных зубов с радиальной ориентацией гранул «НАНОНТС» в качестве каркаса периодонтальных связок, благодаря чему излеченные таким методом зубы способны нести значительную функциональную нагрузку (рис. 3 а — б).
- Рис. 3а. Результаты лечения деструктивных периодонтитов 13 и 23 зубов композитом «НАНОНТС»: пациентка К., 58 лет. DS: хронический гранулематозный периодонтит 13 зуба. DS: хронический гранулематозный периодонтит 23 зуба
- Рис. 3б. Результаты лечения деструктивных периодонтитов 13 и 23 зубов композитом «НАНОНТС»: пациентка К., 59 лет. Через год по завершении лечения R13 и R23 окружены рентгеноконтрастным «НАНОНТС», интегрировавшим с периодонтом причинных зубов.
Через три года по завершении лечения вокруг корней леченных 13 и 23 зубов «НАНОНТС» интегрировал с периодонтом зубов, выстроился сообразно с линиями силового натяжения, по которым ориентированы волокна связочного аппарата в норме. Нет прилегания композита к корням зубов, отмечавшегося в первые месяцы после лечения.
Функциональность интеграции частиц «НАНОНТС» с окружающими тканями
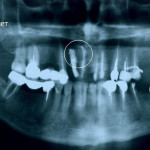
Гранулы никелида титана четко ориентируются в костной ткани и в периодонте по линиям силового напряжения как на нижней, так и на верхней челюсти, что опровергает чисто гравитационный характер интеграции «НАНОНТС» с костной тканью (рис. 4 а, б).
- Рис. 4а. Пациентка К., 58 лет. Представлен результат лечения 23-го зуба через 3 мес. после введения в прикорневой очаг деструкции композита «НАНОНТС». Композит определяется как периапикальный конгломерат овальной формы.
- Рис. 4б. Пациентка К., 61 год. Результат лечения 23-го зуба через 3 года. Гранулы «НАНОНТС» интегрировали с периодонтом зуба с ориентацией частиц по направлению волокон периодонта с образованием композита «НАНОНТС-периодонт». Распределение частиц — сферическое, наиболее благоприятное для демпфирующей функции периодонта. Костная ткань вокруг композита «НАНОНТС-периодонт» имеет повышенную плотность.
Взаимодействие компаунда «НАНОНТС» с имплантатами
В ходе проведения имплантации непосредственно перед установкой имплантата в имплантационное ложе вводится «НАНОНТС». В дальнейшем вокруг установленного имплантата образуется оболочка из геля толщиной в несколько десятков микрон, которая в течение одной-двух недель преобразуется в плотное тело, окружающее имплантат и прочно с ним скрепленное. В то же время материя, образованная из геля в зоне интерфейса имплантат — кость, прочно сцеплена с костной тканью челюсти. Концентрация частиц никелида титана по мере самосборки интерфейса меняется и становится выше в области, примыкающей к костной ткани. В эту область устремляются и частицы гидроксиапатита. Частицы же серебра равномерно распределяются по всему объему [6].
При лечении адентии и деструктивных периодонтитов в комплекном лечении наряду с дентальной имплантацией типовыми сертифицированными ДИ с ЭПФ с целью восстановления всех биомеханических параметров тканей пародонта за счет увеличения корневой части зуба с помощью имплантата, введенного через зуб в костную ткань, нами проводилась эндодонто-эндоссальная имплантация (ЭЭИ) имплантатами с ЭПФ [16].
Вокруг имплантата образуется оболочка из геля толщиной в несколько десятков микрон, которая преобразуется в плотное тело, окружающее имплантат и прочно с ним скрепленное
ЭЭИ никелид-титановыми имплантатами с памятью формы позволяет укреплять корни зубов с последующим протезированием. С этой целью в корень зуба (во внутрикорневой и костный каналы) вводят композит «НАНОНТС». Затем в корень зуба вводится охлажденный в жидком азоте ЭЭ-имплантат [19]. После проведения операции, при нагреве имплантата до температуры тела, ЭЭ-имплантат в силу ЭПФ восстанавливает заданную при нагреве форму. В дальнейшем на наддесневую головку имплантата навинчивается абатмент и проводится ортопедическое лечение по обычной методике.
Следует подчеркнуть, что введение во внутрикорневой и костный каналы геля-композита «НАНОНТС» перед введением ЭЭИ способствует также разрешению т. н. проблемы последней мили, выражающейся в возрастании пристеночного сопротивления по мере продвижения имплантата в корневом и в костном каналах.
Комбинация ЭЭИ с нанофазными биокомпозитами позволяет добиться положительного результата в лечении подавляющего большинства случаев деструктивных периодонтитов на выраженных стадиях деструкции периодонта и прилегающей костной ткани пародонта причинных зубов независимо от возраста больного [9].
После введения в кость имплантат воссоздает как внутрикостную структуру, то есть замещаемый корень зуба, так и наддесневую часть зуба, то есть его коронку [8].
В последующем отмечалась интеграция «НАНОНТС» с костной тканью и замещение костных вакансий органотипом с нормальной плотностью, а непосредственно вокруг имплантата образовывался переходный композит — периимплантат с правильной радиально-сферической ориентацией гранул «НАНОНТС» вокруг имплантата с градиентной плотностью.
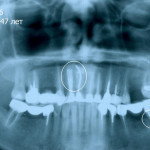
Образование таких бионеорганических композитов нами выявлено, в частности, в ходе комплексного лечения пациентки Д. по поводу пародонтоза с сопутствующими ему адентией и деструктивным периодонтитом (рис. 5 а — д).
- Рис. 5а. Пациентка Д., 46 лет. По поводу адентии 12 и хронического гранулематозного периодонтита 11 проведена имплантация комбинацией ДИ [12] и ЭЭИ [11]. Плотность кости вокруг имплантатов понижена по сравнению с окружающей ДИ и ЭЭИ костной тканью. Над R 11, вокруг имплантата округлая зона просветления костной ткани диаметром 10 мм.
- Рис. 5б. Пациентка Д., 47 лет. После проведения инъекционной остеопластики «НАНОНТС» в участки разрежения кости над R 11 композит сконцентрировался в одной точке, непосредственно прилегая к основанию спирального надкорневого участка ЭЭ-имплантата.
- Рис. 5в. Пациентка Д., 47 лет. В результате проведения инъекционной остеопластики «НАНОНТС» в участки разрежения костной ткани вокруг R 11 и ЭЭ-имплантата образовался переходный композит с правильной радиально-сферической ориентацией гранул и частиц никелида титана с градиентной плотностью.
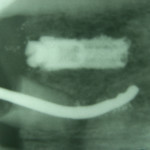
- Рис. 5г. Пациентка Д., 46 лет. Через корень 11 зуба произведена чрескорневая имплантация имплантатом с памятью формы.
- Рис. 5д. Пациентка Д., результат через 2,5 года после проведения инъекционной остеопластики «НАНОНТС» в участки разрежения костной ткани вокруг R 11 и ЭЭ-имплантата. «НАНОНТС» сферически ориентирован вокруг имплантата с метаплазией периодонта в бионеорганический буферный композит, ориентированный по силовым линиям и выполняющий функцию демпфера, присущую периодонту.
В очаги деструкции костной ткани при лечении деструктивных периодонтитов, периимплантитов при лечении пародонтоза с целью укрепления костной ткани композит «НАНОНТС» вводился нами инъекционно, через надкостницу, после проведения предложенной нами инъекционно-аспирационной методики обработки очагов деструкции и замещения замкнутых дефектов костной ткани челюсти [15].
Через 5 месяцев после ЭЭИ в очаг деструкции над R 11 инъекционно был введен гель-композит «НАНОНТС» с одновременной аспирацией содержимого очага деструкции (после соответствующей обработки) по разработанной методике.
Частицы композита «НАНОНТС» в течение трех-четырех месяцев группируются в костной ткани вокруг испытывающего наибольшие функциональные нагрузки спиралевидного участка ЭЭ-имплантата, выполняющего функцию демпфера. В примере таким участком ЭЭ-имплантата является переход прямой внутрикостной части ЭЭ-имплантата в спираль.
Через 14 месяцев после лечения 45 зуба по поводу кистогранулемы с заапикальным выведением «НАНОНТС», лечения тяжелого пародонтита в области 14 и 15 трехкратным инъекционным введением комбинации «НАНОНТС» с ГАНГ и с коллагеновой губкой образовались композиты «НАНОНТС-кость», «НАНОНТС-периодонт».
В течение 2—3 лет идет полная интеграция никелида титана с костной тканью и замещение костных вакансий органотипом с нормальной плотностью
Через шесть месяцев после проведения инъекционной остеопластики композитом «НАНОНТС» его частицы образовали сферу вокруг корня зуба и испытывающего наибольшие функциональные нагрузки спиралевидного участка ЭЭ-имплантата с метаплазией периодонта в гетерофазный буферный бионеорганический композит, ориентированный по силовым линиям и выполняющий функцию демпфера во вновь образованной системе корень — имплантат — кость.
В течение двух-трех лет наблюдается полная интеграция частиц никелида титана с костной тканью и замещение костных вакансий органотипом с нормальной плотностью, а непосредственно вокруг имплантата образуется переходный композит с правильной радиально-сферической ориентацией частиц никелида титана с градиентной плотностью.
Через шесть лет бионеорганический композит успешно справляется с возложенной на него организмом функцией.
Таким образом, образовавшаяся в организме в результате интеграции «НАНОНТС» с тканями организма бионеорганическая структура является функциональной, т. е. наилучшим образом выполняющей только ей присущую функцию в соответствующем локусе. В результате взаимодействия «живой» и «неживой» составляющих биокомпозита «НАНОНТС» с тканями реципиента образуется функциональный фрактальный бионеорганический композит. Такие бионеорганические композиты, образуемые организмом в результате лечебного введения в очаги тканевой деструкции геля «НАНОНТС», путем самоорганизации и самосборки, условно названы нами фениксонами (по аналогии со способностью мифологической птицы феникс к самовозрождению).
Фениксон-репаративно-регенеративная функционально-структурная бионеорганическая тканевая единица Фениксон образуется в месте и в результате проведения инъекционной гетерофазной имплантации геля «НАНОНТС» и функционально интегрируется в окружающую органотипную ткань (рис. 5е).
Выводы
- Комбинация чрескорневых и традиционных зубных имплантатов с нанофазными биокомпозитами типа «НАНОНТС» позволяет добиться положительного результата в лечении большинства случаев деструктивных периодонтитов на выраженных стадиях деструкции периодонта и прилегающей костной ткани пародонта и способствует ускоренной интеграции зубных имплантатов и их пожизненной функциональной эксплуатации, а в случаях адентии позволяет имплантатам функционировать при выраженной атрофии костной ткани.
- Использование функциональных биоматериалов в качестве конструкционных активирует процессы органотипической регенерации и посттравматической репарации с образованием гетерофазных композитов (фениксонов) типа «НАНОНТС-периодонт», «НАНОНТС-кость» и буферного композита типа «Периимплантат».
- Методы наноструктурирования, улучшающие физико-механические свойства сплава и частиц никелида титана оптимизируют интеграцию гетерофазных имплантатов с тканями пародонта.
- Образование фениксона в патологически измененной ткани способствует функциональной перестройке окружающей патологический очаг ткани с взаимодействием ее с вновь образуемым фениксоном.
- Модифицирующая способность наночастиц обеспечивает ускорение интеграции ткани и имплантата, ускоряет процессы репарации и регенерации ткани, замедляет процессы тканевого старения, локального остеопороза, гипотрофии, предупреждает атрофические процессы в тканях.
- Образование фениксонов предупреждает развитие адаптационной болезни и обеспечивает адаптацию тканей к функциональным нагрузкам [20].
Список литературы находится в редакции.