Применение кариеспрофилактических препаратов для местной профилактики кариеса зубов
Г. М. Флейшер
врач-консультант, ГУЗ «Областная стоматологическая поликлиника — Стоматологический центр», двукратный рекордсмен Мировой книги рекордов Гиннесса (Липецк)
Применение кариеспрофилактических препаратов является на сегодняшний день одним из немногих научно обоснованных и доказанных методов эффективной фторпрофилактики. Расширение наших знаний и понимания механизмов защитного действия фторидов во многом изменило отношение к различным методам фторпрофилактики.
Использование кариеспрофилактических препаратов гигиены полости рта в настоящий момент составляет основу любой кариеспрофилактической программы как на индивидуальном, так и групповом, коммунальном уровнях.
Ряд инновационных подходов, таких как использование органических фторидсодержащих соединений и слабокислый водородный показатель применяемого средства гигиены полости рта, позволяет значительно усилить их кариеспрофилактическое и реминерализирующее действия.
Широкое распространение в стоматологии получили препараты фтора, предложенные в 1939 году и успешно применяемые до настоящего времени (Маркскорс Д., 2003). Действие препаратов фтора основывается на образовании кристаллов CaF2 и фторапатита с более стойкой к действию кислот кристаллической решеткой. Ионы фтора и их роль в повышении резистентности эмали и дентина — это десятилетия исследований и тысячи публикаций.
Результат — с каждым годом соединения фтора все более эффективны при лечении и профилактике различных заболеваний и патологических состояний зубов (M. Nanaka, K. Matsunaga, Y. Kadoma, 2000). Соответственно, широко распространенные стратегии профилактики кариеса направлены на встраивание фторида в структуру эмали, в первую очередь, на этапах формирования зубов до их прорезывания.
К числу наиболее распространенных методов системной (или эндогенной) фторпрофилактики, призванных повышать долю фторидсодержащих апатитов в структуре эмали, относятся применение фторида в таблетках и фторирование питьевой воды. Клинические исследования, подтверждающие вышеназванную концепцию, опираются на три группы клинических исследований:
- кариеспрофилактический эффект системного назначения фторидсодержащих препаратов в период беременности;
- изменение интенсивности кариеса зубов у детей, проживающих в регионах фторирования питьевой воды;
- «снижение растворимости эмали зубов за счет встраивания фторидов в гидроксилапатит эмали — основополагающее условие эффективности фторпрофилактики».
Так, Glenn et al, 1982, продемонстрировал взаимосвязь между приемом фторидсодержащих препаратов в период беременности и снижением интенсивности кариеса временных (молочных) зубов. В ряде клинических исследований было продемонстрировано достоверное снижение интенсивности кариеса временных и постоянных зубов у лиц, проживающих в регионах фторирования питьевой воды (Thylstrup et al, 1982; Newbrun, 1989; Ripa, 1993).
Известно, что на поверхности зуба происходят динамические процессы де- и реминерализации, при которых решающую роль играют концентрации ионов Ca2+, РО43—, ОН— в ротовой жидкости и эмали зуба, а также значение рН слюны и межзубного пространства (Боровский Е. В., Леонтьев В. К., 1991; Леонтьев В. К., 1978, 1980; Пахомов Г. Н., 1982).
Было установлено, что проницаемость различных слоев интактной эмали неодинакова. Наименее проницаем поверхностный сдой, затем подповерхностный и средний (Zero D. T., 1999). При усилении процессов деминерализации наблюдается увеличение проницаемости эмали, в том числе и доля органических кислот (Боровский Е. В., Кузьмина Э. М., Немецкая Т. И., 1986; Вожов Е. А.1983; Feamhead R. W., Kawasaki K., Inoue K., 1982).
Воздействие органических кислот приводит к увеличению микропространств эмали, что, в свою очередь, вызывает прогрессию проницаемости и дальнейшее увеличение растворимости эмали. Кроме того, динамическому равновесию процессов де- и реминерализации способствует непостоянство минерального состава эмали за счет способности кристаллов к ионному обмену (Morphis T. L., Tuomba K. J., Lygidakis N. A., 2000; Rosin-Grget K., Lincir I., 2001).
По данным М. Neuman (1961), каждый кристалл покрыт мощным гидратным слоем, позволяющим протекать обмену ионов. Гидратная оболочка указывает, что кристалл электрически заряжен и может содержать чужеродные ионы (Пахомов Г. Н., 1982; Curzon M. J., Losee F. L., 1977). Кроме того, гидратная оболочка является источником ионов, участвующих в обменных и заместительных реакциях с ионами поверхностных и глубоких слоев кристаллической решетки гидроксиапатита (Rosin-Gаget K., Lincir I., 2001).
Процесс проникновения ионов в эмаль зависит от ионного радиуса, активности, химических свойств и концентрации ионов. Важно также состояние поверхности гидроксиапатита, заряд и концентрация ионов на поверхности гидратного слоя. Большинство неорганических ионов по своей величине меньше толщины гидратного слоя, поэтому они легко проникают и накапливаются в нем (Пахомов Г. Н., 1982; Driessens F. M., 1982).
Установлено, что процесс проникновения ионов увеличивается при прогрессировании очаговой деминерализации, что служит основой процесса реминерализации (Боровский Е. В., Кузьмина Э. М., Немецкая Т. И., 1986; Боровский Е. В., Леонтьев В. К., 1991; Пахомов Г. Н., 1974; Driessens F. M., 1982). Предметом особого обсуждения является вопрос содержания фтора в реминерализующих растворах.
Введение в состав реминерализующих растворов ионов фтора в несколько раз усиливает процесс реминерализации (Тищенко Л. Ю., 2009). Gonzales М. (1998) показал, что фтор увеличивает скорость включения в эмаль кальция и фосфора. При содержании фтора 0,1 мг/л, что является низкой концентрацией, происходит преципитация апатита из нестойких пересыщенных растворов, каким является слюна.
При отсутствии фтора кристаллы апатита не преципитируют из насыщенных растворов. В таком случае происходит формирование растворимых субстанций, каким является октакальцийфосфат (Knappwost A., 1952; Mount J., 2003).
Однако добавление в реминерализующие растворы фтора приводит к соединению его с кальцием и образованию нерастворимого вещества, не оказывающего влияния на структуру эмали.
Ряд современных экспериментальных данных свидетельствует о том, что ключевая роль в реализации кариостатических механизмов действия фторидов принадлежит, в первую очередь, не максимальному содержанию фторапатита в эмали, а присутствию ионизированного фторида в среде, окружающей эмаль зуба.
В исследованиях in vitro и in situ показано, что ключевой механизм противокариозного действия фторидов связан с регулированием кинетики де- и реминерализации. Согласно современным представлениям, ионизированные фториды обеспечивают противокариозный эффект за счет следующих механизмов:
- препятствие (замедление) деминерализации интактной эмали;
- влияние на кинетику реминерализации деминерализованной эмали;
- оптимизация кристаллического состава эмали (за счет фторида кальция и фторапатита).
Эффект подавления деминерализации эмали в присутствии ионизированного фторида в окружающей среде носит подтвержденный дозозависимый характер, что открывает значительные возможности для совершенствования методов местной фторпрофилактики путем повышения концентрации ионизированного фтора в средах, непосредственно контактирующих с эмалью (в т. ч. в микробной биопленке), по сравнению с биологической жидкостью полости рта.
Стимуляция и ускорение реминерализации связаны с низкой растворимостью фторапатита, который начинает восстанавливаться даже в слабокислой среде раньше, чем остальные фазы апатита эмали. Следовательно, в ходе реминерализации, развивающейся после воздействия кислоты, происходит перераспределение минеральных фаз эмали, при этом доля стабильных апатитов повышается, а доля легкорастворимых фаз фосфата кальция снижается (Соловьева А. М., 2009).
Реминерализация эмали зуба возможна только при сохранении функции органических матриксов эмали, состоящих из белков, глюкопротеидов, липидов (Максимовский Ю. М., Земскова М. И., 1994).
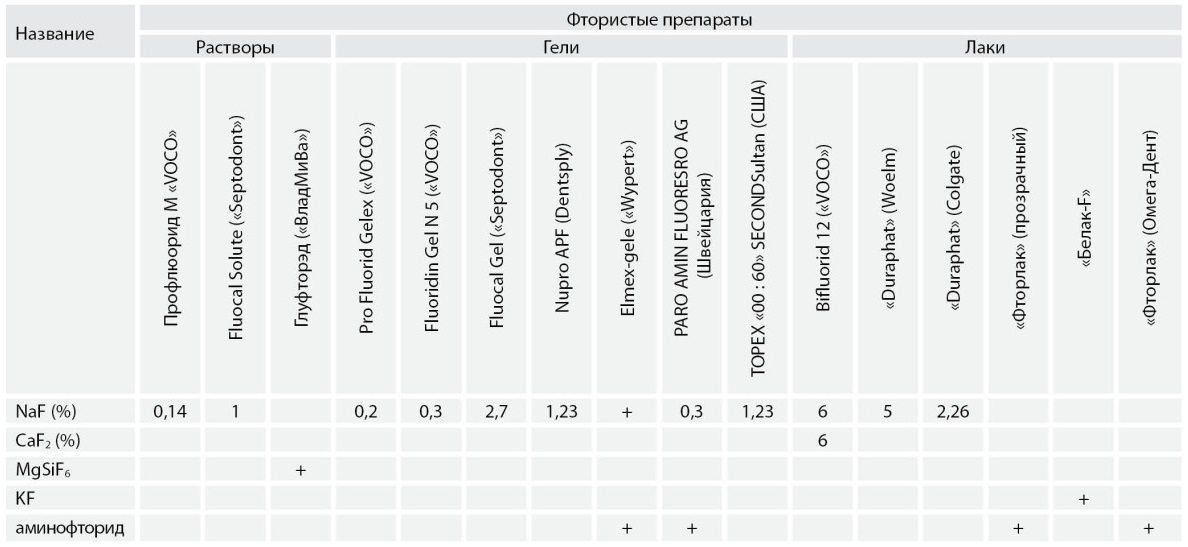
Для успешного лечения применяют кариеспрофилактические и фтористые препараты (табл. № 1), которые восполняют дефекты кристаллической решетки, повышают резистентность эмали к действию кислот, понижают ее проницаемость.
I. Фтористые препараты:
А. Фторсодержащие растворы:
- Pro Fluoride M («VOCO»),
- Fluocal Solute («Septodont»),
- «Глуфторэд» («ВладМиВа»).
Б. Фторсодержащие гели:
- Fluocal Gel («Septodont»), Fluoridin Gel N 5 («VOCO»), Pro Fluorid Gelex («VOCO»), Fluor-Gel («Blend-a-med»), Oral В Fluor-gel («Cooper»), Elmex-gele («Wypert»), PARO AMIN FLUOR ESRO AG (Швейцария), Flor-Opal (Ultradent Product Inc., США), TOPEX «00 : 60» SECOND Sultan (США), Nupro APF (Dentsply).
В. Фторсодержащие лаки:
- Fluoridine («VOCO»), Bifluorid 12 («VOCO»), ADMIRA PROTECT («VOCO»), Multifluorid («VOCO»), Controcar («Hammacher»), Duraphat («Woelm»), «Fluor Protector», «Composeal», DuraShield® (Sultan chemists inc. США), лак белый стоматологический Flor-Opal Varnish White (Ultradent Product Inc., США), Colgate «Duraphat» с фторидом натрия, «Duraphat» (Woelm).
- «Белагель F» («ВладМиВа»), «Фторлак» (Phthorlacum), «БЕЛАК F» («ВладМиВа», Россия), «Фторлак» («Омега-Дент»), лак «Стомафтор», «Фторлак» (прозрачный), «Фторлак» бесцветный, «РАДОГЕЛЬ F Радуга-Р» (Россия), «ПРОФИЛАК» («СтомаДент», Россия).
II. Реминерализирующие препараты:
- Белагель Са/Р («ВладМиВа»),
- эмальгерметизирующий ликвид (Humanchemie, Германия),
- «Ремодент» (Латвия),
- GC Tooth Mousse (Япония),
- MI PASTE PLUS (GC), фирма Dental Resources (США):
- реминерализующий гель со фтором и кальцием,
- фтористое полоскание (концентрат).
Показания к применению кариеспрофилактических препаратов:
- на терапевтическом приеме (при лечении кариеса в стадии пятна, множественного кариеса зубов, кариеса корня, гиперестезии твердых тканей, клиновидных дефектов, для обработки реставраций после шлифования и полирования, при патологической стираемости зубов и т. д.);
- на ортопедическом приеме (после проведения пришлифовывания зубов, для защиты живой культи отпрепарированного зуба, при обработке контактных поверхностей соседних зубов, перед цементировкой временных и постоянных коронок на живые зубы, при фиксации кламмерных конструкций и т. д.);
- на пародонтологическом приеме (после кюретажа пародонтальных карманов для защиты шеек зубов, при цервикальной гиперестезии и т. д.);
- подростковый возраст — при лечении и профилактике кариеса у детей (сохранение молочных зубов, при наличии пигментированных глубоких фиссур постоянных зубов, в стадии созревания фиссур, при незрелых фиссурах и т. д.);
- на ортодонтическом приеме (за один месяц до начала ортодонтического лечения, при фиксации и снятии брекетов, колец);
- восстановление минерального состава эмали после проведения процедуры отбеливания;
- завершающий этап после «Дентилюкса» или профессиональной гигиены полости рта;
- период беременности.
Воздействие фторидов на метаболизм бактерий зубного налета
Данные по влиянию фтористых соединений на состав микробной флоры зубного налета противоречивы. Так, одни авторы указывают на снижение Str. Murans по сравнению с другими микроорганизмами зубного налета (Loesche W. J., Syed A. A., Murray R. G., Mellberg J. R., 1976). В некоторых работах значительных изменений микробной флоры выявлено не было (Marsh P. D., 1999).
Обнаружено влияние фтора на барьерную функцию клеточных мембран микроорганизмов (Edgar W. M., Cockburn M. A., Jenkins G. N., 1981; Wendt L. K., Koch G., Birkhed D.,2001). Предполагают, что посредством изменения электрического потенциала клеточной мембраны свивается поступление сахаров, а также ионов К+ и РО43— в микробную клетку (Eisenberg A. D., Marquis R. E., Bender A. D., 1980).
Снижение ионов К+ вызывает депрессию продукции кислоты микроорганизмами (Geddes D. A. M., Nee S. G., 1982; Marsh P. D., 1999). При присоединении к иону фтора Н+ иона образуется молекула HF, она легко проходят через мембрану и диссоциируется в цитоплазме на Н+ и F— (Luoma H., Luoma A. R., Seppa L., 1984). Высвобождение протона способствует снижению рН цитоплазмы, а фтор ион непосредственно может ингибироватъ процесс гликолиза и синтез кислот микроорганизмами, что в конечном счете приводит к бактериолизису (Broukal Z., Zajicek O., 1974).
Кроме того, некоторые авторы считают, что фториды способны влиять на адгезию бактерий зубного валета к эмали зуба за счет нарушения формирования экстрацеллюлярных полисахаридов — субстанции, играющей основную роль в бактериальной адгезии (Brudevold F., Naujoks R., 1978; Ferreti G. A., Tanzer J. M., Tinanoff N., 1982). Также фториды замедляют образование липотеихоновой кислоты, отрицательно влияя на способность бактерий к адгезии на поверхности зуба.
Фтор оказывает влияние на различные стадии метаболизма бактерий зубного налета, особенно на обмен углеводов и, в частности, процессы гликолиза. При этом происходит угнетение активности фермента энолазы. Под воздействием энолазы фосфоэнолглицерат превращается в фосфоэнолпируват. Активность энолазы зависит от наличия свободного магния. Ионы фтора связываются с магнием, что приводит к угнетению активности энолазы.
Фтор также замедляет процессы транспортировки глюкозы в бактериальные клетки. Проникание глюкозы в клетку стрептококка может осуществляться двумя путями. Посредством системы фосфоэнолпируват-фосфотрансферазы (ФЭП-ФТФ) образуется глюкоза-6-Р, проникающая внутрь клетки.
При этом из фосфоэнолпирувата образуется активированный фосфат. Фтор оказывает косвенное угнетающее действие на внутриклеточный синтез полисахаридов, поскольку в связи с прекращением функционирования механизма ФЭП-ФТФ замедляется образование необходимой для синтеза полисахаридов глюкозы или этого процесса не происходит. На распад внутриклеточных резервных углеводов фтор не влияет.
Как уже упоминалось, фториды угнетают образование фосфоэнолпирувата. При низком значении рН во внеклеточном пространстве ионы фтора соединяются с протоном и в виде HF проникают внутрь клетки. Значение протонного градиента снижается, и в результате уменьшается транспортный поток глюкозы. Вследствие диссоциации HF во внутриклеточном пространстве происходит снижение значения рН. Поскольку ферменты гликолиза проявляют наибольшую активность в щелочной среде, снижение рН угнетает метаболизм бактерий (Хельвиг Э., Климек Й., Аттин Т., 1999).
Таким образом, в обычных физиологических условиях фторсодержащие соединения в незначительной степени влияют на бактерии зубного налета, но, воздействуя на процессы метаболизма зубного налета, могут изменять его микробный состав.
Механизм противокариозного действия фтора
При наилучших условиях, то есть когда человек получает оптимальное количество фтора в течение всей жизни, могут реализоваться следующие звенья в сложном механизме противокариозного действия фторидов.
Первое звено — во время образования органической матрицы и ее первичной минерализации. Оптимальное поступление фтора в этот период способствует синтезу матрицы, образованию кристаллов и процессу минерализации.
Второе звено — после окончания деятельности амелобластов в длящейся несколько лет преэруптивной стадии, когда коронки зубов химически еще нестабильны. Вследствие относительно легкого замещения гидроксила фтор-ионом кристаллическая решетка эмали обогащается фторапатитом с образованием более устойчивых к физическим, химическим и биологическим воздействиям структур. Поэтому считается, что второе звено противокариозного действия фторидов имеет даже большее значение:
Ca10(PO4)6(OH)2 + F– à Ca10(PO4)6F(OH) + (OH)– (1)
В результате реакции изомерного замещения из гидроксиапатита получается гидроксифторапатит. Это соединение обладает значительно большей резистентностью к растворению, чем гидроксиапатит. При замещении фтором даже одной из 50 гидроксильных групп растворимость эмали резко снижается. Однако при действии высоких концентраций фтора на гидроксиапатит реакция идет по другому типу:
Ca10(PO4)6(OH)2 + 20F– à 10СаF2 + 6PO43– + 2(OH)– (2)
В результате этой реакции образуется фторид кальция — практически нерастворимое соединение, которое быстро исчезает с поверхности зуба в результате выщелачивания. Эта реакция при фторировании является нежелательной, в связи с чем не следует применять высокие концентрации фторидов, особенно в кислых растворах.
Третье звено — в постэруптивном периоде, когда ионный обмен значительно замедляется; в этой стадии фторсодержащая вода и несколько обогащенная фтором слюна, омывая коронку зуба, поддерживают барьерные свойства поверхностных слоев эмали и, возможно, способствуют ее реминерализации (Лошакова Л. Ю., 2011).
Механизм действия фтористых препаратов на эмаль зубов
Основным принципом реминерализации является возмещение убыли минеральных элементов в деминерализованных твердых тканях, которые обеспечивается повышением проницаемости последних для ионов и молекул лекарственных средств.
При реминерализирующей терапии растворимость эмали меняется двухфазно: вначале наступает быстрое увеличение растворимости эмали со значительным снижением избыточного выброса Са2+. Через шесть месяцев растворимость эмали вновь уменьшается и наступает равновесие процессов де- и реминерализации (Максимовская Л. Н., 2002).
Rolla G. (1988) изучал влияние фторида кальция, формирующегося на деминерализованной поверхности эмали зуба. Было выяснено, что CaF2 способствует увеличению резистентности эмали путем блокирования путей диффузии во время кислотной атаки.
Однако из-за достаточно крупного размера молекулы фторида кальция неспособны долго сохраняться на поверхности зуба и, соответственно, длительно препятствовать деминерализации и усиливать реминерализацию (Rosalen P. L., Pearson S. K.,
Bowen W. L., 1996).
Механизм местного действия фтористых препаратов на эмаль зубов заключается в их включении в кристаллическую решетку эмали. При этом гидроксил или другой менее активный ион замещается на F—, что приводит к образованию более устойчивого к кислотному растворению вещества (Knappwost A., 1978; Тищенко Л. Ю., 2009). Установлено, что после аппликаций раствора фтора, подкисленного фосфатом, происходит адсорбция фтора в виде кристаллов CaF2 на органической субстанции эмали.
При воздействии фторидов в количестве 0,1—1,0 мг/л на поверхности эмали формируются фосфаткальциевые комплексы, тонкий слой фторапатита (Ganss C., 2001). Воздействие растворов, содержащих фториды в количестве ниже 0,5 мг/л, ведет к формированию главным образом фторапатита, ускоряя реминерализацию. Растворы, содержащие фториды более 0,5 мг/л, приводят к формированию на поверхности зубов флюорита (Тищенко Л. Ю., 2009).
При воздействии на поверхность эмали комбинаций 8%-ных растворов фтористого натрия и фтористого олова с кислым фосфатом натрия (NaH2PO4) отмечена высокая противокариозная эффективность комбинации фтористого олова с кислым фосфатом. Abrahams L. et al. (Bratthall D., 1995) использовали для реминерализации эмали систему, содержащую фтористый кальций, который служит источником фтора и вместе с кальцием и фосфатами слюны обеспечивает термодинамические движущие силы для образования фторапатита и гидроксифторапатита.
Так, F. Brudevold, R. F. Naujok (1978) указывают, что при использовании фторидов в низких концентрациях образуется фторид кальция и фторапатит, тогда как использование высоких концентраций фторидов приводит, главным образом, к образованию растворимого соединения октокальцийфосфата, неспособного значительно влиять на процесс реминерализации.
Однако, по мнению автора, положительный эффект от воздействия фторидов носит кратковременный характер, снижаясь по мере выхода фтор ионов из эмали (Brudevold F., Naujoks R., 1978). Многочисленные исследования подтвердили, что процесс образования фторапатита идет более интенсивно при использовании фторидов в низких концентрациях (Боровский Е. В., Максимовская Л. Н., Колесник А. Г., 1987; Леонтьев В. К.,1980; Duschner H., Gotz F. L., Ogaard B., 1997; Gibbs C. D., Atherton S. E.,
Huntington E., 1995).
Jenkins G. N. (1988) считает, что ионы фтора, замещая группу ОН— или карбонат, входящий в структуру апатита, воздействуют на формирование кристаллов, увеличивают их размер, а также способствуют процессу реминерализации путем осаждения апатитов из перенасыщенных растворов. В литературе есть сведения, подтверждающие это (Stookey G. К., 1998; Strohmmgei L., Brambilla E., 2001).
Larsen M., Fejersckov O., Tachos B. (1981) выясняли, что постоянное поддержание даже незначительно увеличенной концентрации фтора в полости рта способствует снижению растворимости и содействует процессу реминерализации.
Изменения в эмали при единичном увеличении концентрации фтора слишком малы, но если они поддерживаются продолжительный промежуток времени, то это обеспечивает защиту от выхода кальция и фосфора из поверхностного слоя эмали, а также способствует поступлению ионов фтора в структуру эмали и образованию фторапатита. Этот эффект был достигнут при ежедневном использовании фтористых паст и полосканий (Кузьмина Э. М., 2001; Недосеко В. Б., Ломиашвили Л. М., 1995).
В литературе также есть сведения, что использование фторсодержащих препаратов способствует образованию защитного покровного слоя минеральных компонентов на поверхности эмали, а также в порах разрыхленной эмали при начальных стадиях кариеса.
Эта защитная реакция нарушается, если скорость растворения апатита превышает скорость образования защитного слоя. Фторсодержащие препараты способствуют увеличению скорости образования защитного минерального слоя (Feamhead R. W., Kawasaki K., Inoue K., 1982; Knappwost A., 1978, 1993; Wen H. B., Cui F. Z., Chen X. Q., Wang G., 1995).
Выраженный лечебный эффект фторидов объясняют не только тем, что он способствует повышению накопления ионов кальция и фосфора в поверхностных слоях эмали, но и тем, что в отсутствие фтора кристаллы апатита не приципитируют из насыщенных растворов, а формируют растворимые соединения типа октакальция фосфата. Таким образом, сочетание применения реминерализующих составов и фтора существенно увеличивает эффект их воздействия (Strohmmgei L., Brambilla E., 2001).
Однако при исследовании эмали зуба после аппликаций растворов фторида натрия отмечалось снижение проникновения радиоактивного кальция в глубокие слои эмали по сравнению с поверхностным слоем.
Это свидетельствует о том, что эмаль действует, как ионная мембрана, и плотность отрицательного заряда на поверхности кристалла увеличивается после местной обработки фтором, который создает более высокую катионную специфичность эмали (Christofersen J., Christofersen M. R., Arends J., Leonardsen E., 1995; Featherstone J. D., 2000; Warren D. P., Chan J. T., 1997).
Фториды влияют на обменные процессы в эмали зуба. В процессе взаимодействия фторидов с эмалью происходит отложение кристаллов апатита на поверхности так называемого защитного слоя, чем и объясняется снижение проницаемости и усиление процессов реминерализации.
Наряду с неорганическими соединениями фтора в последнее время нашли применение и его органические соединения — аминофториды. По мнению многих авторов, они более интенсивно включаются в эмаль, повышая ее резистентность к кислотному растворению, что связано с образованием фтористого кальция (Леус П. А., Смирнова Т. А., Пашинина Е. О., 1980; Хоменко Л., Кононович Е., 1997).
Идея использования аминофторида, как средства местного воздействия, связана с реминерализующим действием фтора и физико-химическими свойствами защиты алифатических аминов. Аминофторид способен защищать эмаль от кислот не только за счет образования CaF2, но и за счет осаждения добавок амина (Колесник А. Г., Пилат Е. Л., 1989; Brambilla E., Tosilli A., Felconi A., Gagliani M., 1997; Faller R. V., 1995).
Ряд авторов (Смирнова Т. А., 1984; Jungo Markus, 2001) применял для реминерализации аппликации 1%-ного геля фтористого натрия. Они считают, что механизм профилактического действия фтористого геля заключается в ингибировании лактата и ацетата бактериями зубного налета.
Большинство исследователей указывают на высокую эффективность при использовании фторлаков и фторгелей на гладких поверхностях (Бахмудов Б. Р., 1994; Кузьмина Э. М., Смирнова Т. А., 2001; Маслак Е. Е., Казанцева И. А., Фурсик Т. И., Огонян В. Р., 1997).
Применение фторидов в форме гелей и лаков имеет ряд преимуществ. Они обладают выраженной адгезией к эмали, легко наносятся и способны сохранятся на эмали до 24 часов (Колесник А. Г., Пилат Е. Л., 1989; Кузьмина Э. М., 2001; Attin T., Hartmann O., Hilgers R. D., Hellwig E., 1995).
Однако в докладе экспертов ВОЗ (1995) указывается, что высвобождение фторидов носит «взрывной», кратковременный характер. Для медленного высвобождения фторидов также используют специальные мембраны. Продолжительность выброса фторидов при этом может составлять 30—80 суток. Эти способы, вероятно, могут играть важную роль в профилактике и лечении кариеса в будущем, однако в настоящее время нет исчерпывающих данных по клиническим испытаниям (Castioni N., Beahni P. C., Gurny R., 1998).
Несмотря на различные подходы по использованию фторидов в полости рта, многочисленные данные свидетельствуют, что эффект их воздействия не превышает 45—56 %.
Анализируя литературные данные, можно сделать вывод, что различные соединения фторидов достаточно широко используются для профилактики кариеса зубов. Однако эффективность простых фторидов носит кратковременный характер и требует длительного и частого применения для достижения выраженного профилактического эффекта.
Избыток углеводистой пищи и простых сахаров приводит к увеличению вязкости слюны, что значительно снижает ее минерализующие свойства. По мнению некоторых авторов, вязкая слюна препятствует смыванию кислот брожения с пунктов задержки остатков пищи на зубах, что вызывает усиление процессов деминерализации эмали.
Кроме того, при углеводистой нагрузке отмечалось снижение функциональной активности слюнных желез, изменение физико-химических свойств слюны: уменьшение скорости тока, изменение ее качественного и количественного состава (Круглова Л. Н., Недосеко В. Б., Тер-Никогосова Л., 1988; Сунцов В. Г., 1987; Чекмезова И. В., 1983).
Влияние рН ротовой жидкости на минерализацию эмали
Существенную роль в снижении минерализующей функции слюны играет изменение рН. Считается, что среднее значение рН слюны равно 6,5—7,5, то есть она является нейтральной. Резкое снижение рН наблюдается при углеводистой нагрузке (Боровский Е. В., Бурдина О. В., 1991; Леонтьев В. К., Петрович Ю. А., Круглова Л. Н., 1997; Леус П. А., Лебедева Г. К., 1981).
При изучении влияния сахарозы на состав свойства смешанной слюны у детей было отмечено увеличение вязкости, а также снижение рН ротовой жидкости (Рединова Т. Л., 1989; Токуева Л. И., 1985).
Одним из основных факторов, дестабилизирующих рН ротовой жидкости, является кислотообразующая способность микроорганизмов зубного налета (Балашова Е. И., 1987; Левицкий А. П., Мизина И. К., 1987; Леус П. А., Лебедева Г. К., 1981; Рединова Т. Л., 1989; Mascarenhas A. K., Moursi A. M., 2001).
В работах по влиянию изменения рН слюны на ее состав было доказано, что при снижении рН ниже 5, концентрация ионов водорода снижалась в 10 раз, степень насыщения гидроксиапатитом в 8,3 раза. При этом, по мнению авторов, рН 6—6,62 является критическим. Слюна переходит из состояния минерализующей жидкости в состояние деминерализующей (Боровский Е. В., Леонтьев В. К.,1991; Боровский Е. В., Леонтьев В. К., Максимовская Л. Н., 1984; Gron P., 1983; Larsen M J., 1991).
Наоборот, увеличение рН повышает минерализующие свойства ротовой жидкости вследствие увеличения степени перенасыщения ионами Са2+, НРО42—, F—. Это способствует образованию зубного камня и частично объясняет устойчивость зубов к кариесу в области его образования (Murray I. I., 1986; Navarro M., 2001).
Van Houte J., Lop man J., Kent R. (1996) считают изменение локальной рН основной причиной очаговой деминерализации (Woltgens J. H., Bervouets T. J., Witjes F., Houwink B., 1981). Однако, по мнению других авторов, незначительные колебания локальной рН не могут сильно изменить рН ротовой жидкости в целом (Kanellis M. J.,
2000).
Кратковременное снижение локальной рН в месте воздействия органических кислот зубного налета на эмаль зуба достаточно быстро восстанавливается за счет расхода ионов, содержащихся в ротовой жидкости: Са2+, НРО42—, F—, ОН—. Таким образом, происходит частичное осаждение утраченных ионов и восстановление локального значения рН.
Как отмечалось многими авторами (Леонтьев В. К., 1983; Леонтьев В. К., Чекмезова И. В., Швырногов В. З., 1983; Morphis T. L., Tuomba K. J., Lygidakis N. A., 2000), основным механизмом поддержания постоянства зубных тканей в полости рта является перенасыщенность ротовой жидкости ионами Са2+, НРО42—, F—, другими словами, гидроксиапатитом либо фторапатитом.
A. Knappwost (1993) утверждает, что поверхностный слой эмали покрыт преимущественно ионами Са2+ и РО43—, которые в результате гидролиза в промежуточной стадии образует СаНРО4, а в конечной гидроксиапатит Са10(РО4)6∙(ОН)2. Гидроксиапатит, образующейся на поверхности эмали, в силу слабой растворимости и стабильности может играть защитную роль.
Прогрессия кариеса, таким образом, происходит, когда скорость распространения кариозного поражения выше, чем скорость образования гидроксиапатита покровного слоя (Knappwost A., 1993).
Доказано, что кариеспрофилактическое действие молибдена и алюминия обусловлено подавлением выхода кальция из эмали при воздействии кислот и стимулированием включения фтора в решетку гидроксиапатита (Kleder C. J., Putt M. S., 1984), кроме того, хлорид натрия способствует повышению эффективности ионов фтора, а ионы цинка подавляют активность бактерий (Патент РФ № 2157174 от 29.03.1999).
Основным результатом кариесостатического действия фтора считается подавление процесса деминерализации или активирование реминерализации твердых тканей зуба. В полости рта поверхность зуба постоянно подвергается разным воздействиям.
Сразу после прорезывания поверхность зуба с большей или меньшей плотностью покрывается различными микроорганизмами, метаболическая активность которых при наличии соответствующего субстрата может приводить к снижению уровня рН и вследствие этого к индукции процесса деминерализации. Периоды деминерализации могут сменяться периодами реминерализации, если в результате передачи слюной (клиренс) продуктов метаболизма микроорганизмов и субстрата значение рН возрастает.
Эффект реминерализации является наиболее важным из них. Ионы фторида, проникающие в толщу эмали и в ее поверхность, приводят к укреплению эмали, которая становится не только более стойкой к кариозной атаке, но и сама приобретает способность реминерализоваться или залечить начальные проявления кариеса, вызываемые кислотами кариесогенных микроорганизмов. Необходимые для реминерализации ионы фторида обеспечиваются как фторированной водой, так и различными кариеспрофилактическими препаратами, например фтористыми препаратами (табл. № 1).
Таким образом, обобщив имеющиеся в литературе данные, можно сделать вывод, что увеличение вязкости слюны и изменения рН ротовой жидкости в целом, а также резкие снижения локального рН в месте воздействия микробной флоры непосредственно на эмаль зуба приводят к снижению насыщения ее гидроксиапатитом, что нарушает процессы ре- и деминерализации в сторону усиления последнего.
Изменения эмали на ультраструктурном уровне приводят к образованию очага поражения, диагностируемого визуально как кариес в стадии белого пятна.
На основании всего вышесказанного можно сделать вывод, что использование кариеспрофилактических препаратов с оптимально подобранным составом позволяет проводить наиболее эффективную профилактику кариеса как на индивидуальном, так и на социальном уровнях, а использование системных методов фторпрофилактики должно назначаться дополнительно, с учетом ряда особенностей, и соответствовать международно принятым рекомендациям по применению фторидов.
- Завьялова Т. Г. Профилактика и лечение кариеса в стадии белого пятна методом глубокого фторирования [Текст]: автореф. дис. на соиск. учен. степ. канд. мед. наук / Т. Г. Завьялова. — М., 2003. — 19 c.
- Кисельникова Л. П. Перспективы местного применения фторидов в клинической стоматологии [Текст] / Л. П. Кисельникова // Маэстро стоматологии. — 2007, № 2 (26). — С. 18—22.
- Колесник А. Г., Сахарова Э. Б. Средства профилактики кариеса зубов // Медицинская помощь. — М., 1995. — № 6. — С. 43—45.
- Лобовкина Л. А. Профилактика в терапевтической стоматологии — это выгодно! Л. А. Лобовкина, А. М. Романов [Текст] / Новое в стоматологии. — 2007, № 6. — С. 46—49.
- Лошакова Л. Ю. Курс лекций по актуальным вопросам детской стоматологии: учебное пособие / Лошакова Л. Ю., Пылков А. И.; ГОУ ВПО КемГМА Росздрава. — Кемерово: КемГМА, 2011. — 187 с.
- Маркскорс Д. Препарирование зубов для фиксации коронок (главы из монографии) / Д. Маркскорс, Р. Маркскорс // Новое в стоматологии. Для зубных техников. — 2003, № 1. — С. 73—76.
- Пахомов Г. Н. Первичная профилактика в стоматологии. — М., 1982. — 240 с.
- Соловьева А. М. Основы противокариозного эффекта фторидов [Текст] / А. М. Соловьева // Институт стоматологии. — 2009, № 45. — 32—35 с.
- Тищенко Л. Ю. Клиническая оценка и повышение резистентности эмали и дентина при гиперестезии твердых тканей зуба [Текст]: автореф. дис. на соиск. учен. степ. канд. мед. наук/ Л. Ю. Тищенко — Ставрополь, 2009. — 22 с.
- Флейшер Г. М. «Дентилюкс» — профессиональная гигиена полости рта [Текст] / Г. М. Флейшер // Дентал Юг. — 2011, №10. — С. 48—51.
- Хельвиг Э., Климек Й., Аттин Т. Терапевтическая стоматология. Под ред. проф. A. M. Политун, проф. Н. И. Смоляр. Пер. с нем. — Львов: ГалДент, 1999. — 409 с.
- Knappwost A. Eine dringende Aufgade fur die zahnärztliche Praxis Tiefenfluoridierung durch mineralsche Schmelzvesiegelung // Dtsch. Zahnarztl. Ztschr. — 1993, № 8. — Р. 20—23.