Применение препаратов гиалуроновой кислоты в хирургической пародонтологии
Гиалуроновая кислота (ГК) на протяжении многих лет успешно используется в разных отраслях медицины, в частности в ортопедии и эстетической хирургии, широко применяется в косметологии (в кремах, лосьонах, губных помадах) и находит применение в стоматологической практике.
Гиалуроновая кислота является природным полисахаридом, входящим в группу гликозамингликанов. Молекула состоит из повторяющихся звеньев дисахарида D-глюкуроновой кислоты и N-ацетилглюкозамина.
Производить гиалуроновую кислоту способно большинство клеток нашего тела, в особенности клетки соединительных тканей. ГК образуется на клеточной мембране и передается напрямую в межклеточное пространство (матрицу). Почти во всех видах тканей ГК является важным компонентом внеклеточной матрицы.
Функцией гиалуроновой кислоты во внеклеточном пространстве является связывание воды и тем самым обеспечение важных процессов обмена веществ и стабильности структуры ткани.
ГК активирует ингибиторы металлопротеиназ и таким образом эффективно противодействует разрушению тканей. Подобный эффект достигается путем замедления цитокинов, которые вызывают воспаления (TNF α). Тем самым гиалуроновая кислота может способствовать сохранению тканей.
Наиболее известным является применение препаратов ГК в виде инъекций для коррекции и устранения дефектов десневых сосочков, прилегающих к зубам или дентальным имплантатам, уменьшения расстояния между промежуточной частью мостовидного протеза и слизистой оболочкой, покрывающей альвеолярный отросток, а также при отсутствии десневого сосочка (Becker et al., 2009).
По данным Becker et al. (2), благодаря бактериостатическому эффекту, в частности воздействию на микроорганизмы в тканях пародонта, такие как A. actionomyecetemcomitans, Prevotella intermedia и др., гиалуроновая кислота обеспечивает биологическую защиту при хирургическом лечении патологии пародонта.
A. Ballini с соавторами [1] исследовали возможность комбинированного применения этерифицированной ГК и аутогенной кости для хирургической коррекции костных дефектов у пациентов, страдающих пародонтитом. При проведении лоскутной операции после откидывания слизисто-надкостничного лоскута, удаления грануляционной ткани, зубных отложений и обработки поверхности корней и лоскута ручными и ультразвуковыми инструментами смешивали аутокость и препарат гиалуроновой кислоты, заполняли костные карманы, затем ушивали. ГК предотвращает смещение аугментационного материала и обеспечивает стабильность объема.
Вместе с тем данные об антимикробной эффективности препаратов ГК в пародонтологии весьма противоречивы, так, Xu Y с соавторами [3] провел исследование, в котором не было выявлено клинического и микробиологического улучшения при использовании геля ГК в сравнении только с SRP. Помимо традиционных диагностических критериев в исходной ситуации, через 6 и 12 недель исследовались образцы поддесневой биопленки на предмет наличия A. actinomycetemcomitans, Porphyromonas gingivalis, Prevotella intermedia, Tannerella forsythensis и Treponema denticola. Не было выявлено различий между группами, что подтвердило антимикробный эффект гиалуроновой кислоты.
Таким образом, применение гиалуроновой кислоты в стоматологической практике целесообразно в пародонтологии (лечение гингивита, санация пародонтальных карманов, лоскутные операции), однако эффективность применения данного препарата требует дальнейшего изучения.
Целью работы явилось изучение влияния препаратов гиалуроновой кислоты на течение послеоперационного периода у пациентов с хроническим генерализованным пародонтитом после проведения хирургического лечения (открытый кюретаж пародонтальных карманов, лоскутная операция).
Всего проведено обследование и лечение 34 пациентов в возрасте от 35 до 56 лет.
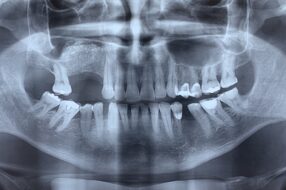
Диагноз — пародонтит средней (23 человек) и легкой (11 человек) степени тяжести — был поставлен на основании клинических и рентгенологических данных.
Все пациенты были разделены на две группы: 1-я — основная, пациенты, у которых наряду с проведением операции использовали ГК в виде Tissue Support и Flex Barrier (20 человек); 2-я — контрольная (14 человек), без ГК.
Tissue Support состоит из гиалуроновой кислоты с простой сетчатой структурой и создан специально для лечения воспаления слизистой оболочки полости рта и для улучшения заживления ран после хирургического вмешательства. Благодаря низкой вязкости гель гиалуроновой кислоты наносится с помощью тупой канюли просто и в любой области (рис. 1).
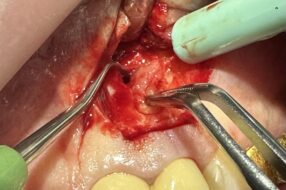
При проведении открытого кюретажа препарат с помощью канюли вводился в пародонтальный карман и контролировалось формирование сгустка. Коагулят стабилизируется благодаря гидрофильным свойствам гиалуроновой кислоты. Далее препарат наносился в зону операции на слизистую оболочку 1 раз в сутки (5 дней) после приема пищи. При лоскутных операциях препарат наносили непосредственно на операционную рану под швы.
Flex Barrier состоит из гиалуроновой кислоты простой сетчатой структуры или поперечно сшитой. Благодаря очень высокой вязкости этот гель гиалуроновой кислоты хорошо наносится и не растекается (рис. 2). Проводили смешивание материала «Остематрикс» и геля Flex Barrier, что оптимизирует процесс в плане распределения аугментата и ускоряет процесс образования новой костной ткани. Применяли при лоскутных операциях.
Контроль в течение послеоперационного периода осуществлялся на основании клинических симптомов (отек, гиперемия, экссудация из раны, боль, состояние региональных лимфатических узлов, кровоточивость), микробиологических данных до операции, спустя 3, 5 и 7 суток после операции, цитологии мазков-отпечатков в сроки 3 и 7 суток.
Для контроля антимикробной эффективности препарата и его влияния на микробиоценоз полости рта проводили микробиологическое исследование. Исследование включало выделение микрофлоры со слизистой оболочки в области линии швов и идентификацию выделенных бактерий с использованием техники анаэробного культивирования. Взятие материала проводили трехкратно:
- до операции (определение исходного фона для контроля и последующего устранения вирулентных штаммов);
- на 3-и сутки (до чистки зубов и обработки препаратами);
- на 7-е сутки (до чистки зубов и обработки препаратами) с поверхности эпителизированной линии разреза.
Посев материала с целью получения изолированных колоний осуществляли секторальным методом в чашке Петри с 5%-ным сердечно-мозговым гемин-агаром, приготовленным на основе Brain-Heart Agar компании Difco (USA). Культивирование анаэробных культур бактерий осуществляли в анаэростате с бескислородной газовой смесью, состоящей из 80 % азота, 10 % водорода, 10 % углекислого газа при температуре 37 °С от 48 часов до 7 дней.
Цитологические исследования проводили методом мазков-отпечатков, мазки окрашивали по Романовскому — Гимзе. Подсчет элементов цитограммы производили с помощью светового микроскопа при увеличении х 400.
Клинически у всех пациентов основной группы уже на 3-и сутки после операции слизистая оболочка альвеолярного отростка и переходной складки в зоне операции имела нормальную окраску, швы были в хорошем состоянии, края ран плотно соприкасались, отделяемого не определялось. В контрольной группе у
6 пациентов слизистая оболочка была гиперемирована, отечна, отделяемое серозное в небольшом количестве. На 7-е сутки в основной группе раны зажили первичным натяжением, края ран эпителизировались. В контрольной группе у 2 пациентов наблюдалось частичное расхождение краев раны в дистальных участках с сохранением небольшого серозного отделяемого.
Такие различия в клиническом течении раннего послеоперационного периода, по нашему мнению, обусловлены рядом моментов: снижением микробной нагрузки в области послеоперационной раны при использовании ГК, осмотическим действием ГК, способностью связывать воду (экссудат), уменьшением числа поврежденных лейкоцитов.
При изучении мазков-отпечатков в области раны на 1-е сутки достоверных различий между количеством лейкоцитов, числом бактериальных клеток и соотношением между живыми и погибшими лейкоцитами не обнаружено. Это, по нашему мнению, обусловлено выделением крови и раневого экссудата из раны, что искажает истинную картину. Поэтому мы провели анализ только на 3-и сутки после операции. Установлено, что в контрольной группе количество лейкоцитов в раневом экссудате был достоверно выше, чем в основной группе: 69,2+1,6 и 41,5+2,5 в 10 квадратах сетки окуляра соответственно (р <0,01), при этом соотношение между погибшими и живыми лейкоцитами было равно 2,14+0,19 к 1,12+0,2, то есть процент живых лейкоцитов составлял 52,3 %, в то время как в основной группе 90,9 %. Микробные клетки в мазке-отпечатке в основной группе располагались как внутриклеточно, так и внеклеточно в небольшом количестве (табл. № 1), в то время как в контроле более чем у половины пациентов их количество было достоверно выше (p<005, p<0,01).
Таблица № 1. Результаты цитологического исследования мазков-отпечатков из раны на 3-и сутки после операции
Показатель |
Основная группаM+m |
Контрольная группаM+m |
Р |
|
Число лейкоцитов в 10 квадратах сетки окуляра |
41,5+2,5 |
69,2+1,6 |
<0,05 |
|
Процент живых лейкоцитов |
90,9+2,5 |
52,3+1,9 |
<0,001 |
|
Процент нейтрофилов с внутриклеточно расположенной микрофлорой |
9,2+1,1 |
13,9+0.7 |
<0,05 |
|
Число микробных клеток в 10 квадратах сетки окуляра (внеклеточно) |
35,0+3,8 |
84,2+3,8 |
<0,01 |
Более низкое число лейкоцитов, при высокой степени сохранения их жизнеспособности и функциональной активности, вероятно, обусловлено положительным влиянием ГК, внесенной во время операции. В пользу этого говорит и более низкое число микробных клеток.
При микробиологическом исследовании определялось достаточно большое количество бактерий, обладающих высоким агрессивным потенциалом: S. aureus, P. melaninogenica, Actinomyces spp., а также грибы Candida spp.
Вместе с тем в основной группе при применении с целью профилактики воспалительных осложнений Tissue Support на 3-и сутки в области линий послеоперационных швов выделяли бактерии — резиденты полости рта.
В то же время количество бактерий, обладающих высоким агрессивным потенциалом, было достоверно ниже, чем в контрольной группе (P<0,05).
На 5-е сутки после операции при бактериологическом исследовании, выполненном у пациентов контрольной группы, определяли некоторое увеличение количества S. sanguis, P. Anaerobius. Отмечали также увеличение обсемененности представителями агрессивных видов микроорганизмов. Такие важные составляющие ассоциации нормальной микрофлоры, как S. salivarius, напротив, в этот период не обнаруживались. Сохранялось выделение Actinomyces spp. и грибов Candida spp.
В основной группе в этот период наблюдалось достоверное снижение микробной обсемененности представителями «стабилизирующих» видов до нормальных цифр.
Отмечали достоверное снижение количества представителей большинства «агрессивных» видов.
На 7-е сутки у пациентов контрольной группы отмечено некоторое снижение обсемененности представителями стабилизирующих видов.
Вместе с тем сохранялось выделение представителей ряда «агрессивных» видов, хотя и в меньшем количестве. Не определяли Prevotella melaninogenica и грибы Candida spp.
Аналогичные тенденции наблюдали и в основной группе. Однако уровень микробной обсемененности представителями «стабилизирующих» и некоторых «агрессивных» видов был достоверно ниже как по сравнению с пациентами основной группы на 5-й день исследования, так и по сравнению с пациентами контрольной группы.
Следовательно, у пациентов основной группы (при использовании ГК) при различных видах пародонтологических вмешательств (кюретаж, лоскутная операция) нормализация микробиоценоза в зоне послеоперационного шва на слизистой оболочке происходила в более ранние сроки, чем у пациентов контрольной группы.
Таким образом, полученные данные свидетельствуют о противомикробном эффекте применения ГК и отсутствии выраженного токсического действия препаратов на нейтрофилы.
Tissue Support и Flex Barrier способствует снижению концентрации пародонтопатогенных микроорганизмов в области послеоперационной раны даже при первичном бактериальном загрязнении (операция на тканях пародонта), что оптимизирует заживление и снижает количество осложнений.