Характеристика титановых имплантатов с биоактивным гидрофильным кальцийфосфатным покрытием
Установка дентальных имплантатов у пациентов с частичной и полной адентией является эффективным методом замещения отсутствующих зубов [1]. За последние десятилетия появилось огромное разнообразие конструкций имплантатов и технических модификаций, созданных для улучшения процессов заживления и предотвращения потери костной ткани.
Согласно литературным данным, существует более 1300 видов дентальных имплантатов, изготовленных из различных материалов, имеющих различные формы, размеры, длину, с различными характеристиками поверхности или покрытия [2].
Высокие показатели остеоинтеграции были отмечены при использовании дентальных имплантатов различных конструкций и марок [3—5]. Первичная стабильность, которая является одним из важнейших критериев интеграции имплантата и показателем успеха на ранней стадии заживления, в основном зависит от анатомической конструкции имплантата (длина, диаметр, форма и резьба), хирургической техники, а также от объема и типа костной ткани [3, 4]. В течение периода остеоинтеграции костная ткань постепенно перестраивается по отношению к резьбе имплантата, в результате чего путем формирования непосредственного контакта костной ткани и поверхности имплантата достигается вторичная стабильность [5].
Она соответствует показателю эффективности имплантата, зависит от модификации его поверхности и ремоделирования кости, индуцированного механическим стрессом в начальной фазе костного заживления [6].
Согласно современной литературе, ведутся дискуссии о способности имплантатов выдерживать раннюю или немедленную нагрузку с целью сокращения времени ожидания для пациента. В дополнение к упомянутым параметрам первичной и вторичной стабильности, остеокондуктивные характеристики имплантата являются факторами, которые влияют на реакцию кости, а также на качество связи костной ткани с поверхностью имплантата [7, 8]. Обработка поверхностей способствует повышению вторичной стабильности после установки за счет стимуляции остеоинтеграции [9, 10, 6]. Были разработаны и испытаны различные способы покрытия имплантатов, например плазменное напыление, осаждение распылением, золь-гелевое покрытие, электрофоретическое или биомиметическое осаждение. Электрохимические методы для изменения исходных характеристик титановых поверхностей являются относительно простыми, недорогими и эффективными методами [11—13]. Кальцийфосфатные (CaP) покрытия хорошо известны в дентальной имплантологии [14, 15] и могут стимулировать остеоинтеграцию имплантата благодаря химическим процессам, происходящим на биологически активной поверхности [16, 17]. На сегодняшний день доступна система имплантатов с полностью резорбируемым и адгезивным кальцийфосфатным (CaP) покрытием (Bioactive®) (рис. 1, 2).
- Рис. 1. Изображение имплантата с CaP-покрытием.
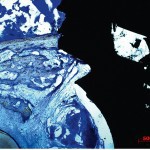
- Рис. 2. Выраженные гидрофильные свойства имплантата с CaP-покрытием.
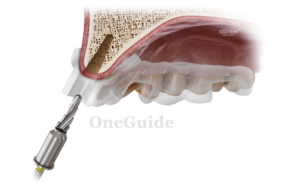
Нанесение покрытия Bioactive® представляет собой электрохимический процесс покрытия имплантатов в водном растворе, содержащем ионы кальция и фосфата. Согласно данным производителей, кальцийфосфатное покрытие обладает следующими свойствами: имеет малую толщину (20—
30 мкм) с большой площадью активной поверхности, стимулирует остеосинтез [18] и способствует замещению покрытия Bioactive® костной тканью непосредственно на поверхности имплантата в течение 6—10 недель после операции. Имплантаты данной системы изготовлены из титанового сплава 5-го класса, имеют пескоструйно обработанную и протравленную поверхность, внутренний шестигранник, коническую форму, самонарезающую резьбу. Кроме того, имплантаты имеют двойную резьбу с глубокой и острой нарезкой, уменьшающейся в направлении плеча имплантата, которая обеспечивает саморетенцию, нацеленную на высокую первичную стабильность. Насколько нам известно, никаких дальнейших клинических исследований, касающихся имплантатов с данной поверхностью, кроме экспериментов на животных, проводимых Рейгстадом и др. [18], опубликовано не было. Таким образом, целью настоящего исследования явилось изучение биологических и хирургических результатов применения дентальных имплантатов с покрытием CaP («Альфа-Гейт», Кафр-Кара, Израиль). Были оценены гистологические данные, разница между первичной и вторичной стабильностью (ISQ) и прочие клинические параметры.
Особенности остеокондуктивности титановых имплантатов с кальцийфосфатным покрытием
Эксперименты были проведены для сравнения остеокондуктивности в области плеча супраальвеолярно установленных имплантатов с кальцийфосфатным (CaP) покрытием и обычных пескоструйно обработанных / протравленных кислотой (SLA) имплантатов. Для проведения рандомизированного исследования типа «split-mouth» четырем кроликам с двух сторон нижней челюсти были установлены CaP- и SLA-имплантаты. Имплантаты были размещены на 2 мм выше альвеолярного гребня.
Через 3 недели в области плеча каждого имплантата был определен процент линейного заполнения костной тканью (PLF), а также проведена оценка контакта костной ткани и имплантата (BIC-D). Через 3 недели вновь образованная костная ткань определялась в области плеча у большинства имплантатов обоих типов (75 %). PLF был значительно выше у имплантатов с CaP-покрытием (11,2 % и 46,5 %; n = 8, p =0,008). BIC-D также был значительно выше у имплантатов с CaP-покрытием (13,0 % и 71,4 %; n = 8, p <0,001) (рис. 3, 4). Результаты данного исследования впервые показали, что поверхности супраальвеолярно установленных имплантатов с кальцийфосфатным покрытием обладают свойствами вертикальной остеокондуктивности и значительно улучшают связь костной ткани с имплантатом в области его плеча.
- Рис. 3 a. Измерение PLF и BIC на оцифрованном гистологическом образце. Вертикальное формирование костной ткани на имплантате с CaP-покрытием
- Рис. 3б. Измерение PLF и BIC на оцифрованном гистологическом образце. Вертикальное формирование костной ткани на имплантате с CaP-покрытием.
- Рис. 4. Плотный контакт костной ткани с поверхностью имплантата.
Клинические исследования
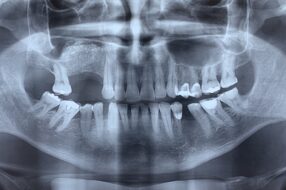
Нами были проанализированы результаты исследования 64 последовательно установленных имплантатов. Все имплантаты относятся к системе Alfa Gate Bioactive («Альфа-Гейт», Кафр-Кара, Израиль). Имплантаты были установлены 24 пациентам. Имплантация проводилась в дистальном отделе нижней челюсти.
Для оценки показателей эффективности и приживаемости имплантатов были определены следующие виды обследований: определение первичной и вторичной стабильности имплантата (резонансно-частотный анализ (ISQ; Osstells Mentor® (Osstell AB, Гетеборг, Швеция) и использование Periotest® (Siemens AG, Бенсхайм, Германия), а также радиодиагностика.
Хирургические процедуры
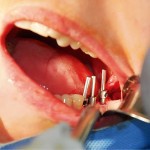
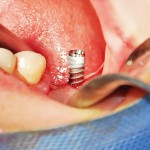
Все операции проводились под местной анестезией с откидыванием лоскута. Препарирование проводилось с помощью низкоскоростных наконечников с высоким крутящим моментом (800 оборотов в минуту) с использованием интенсивной ирригации холодным физиологическим раствором. Тип костной ткани (от I до IV) регистрировался при препарировании каждого нового ложа для имплантата. Все имплантаты устанавливались вручную без погружения, а окончательный торк измерялся с помощью ручного динамометрического ключа (рис. 5—7). Для количественной оценки стабильности имплантатов мы регистрировали ISQ с помощью устройства Osstell Mentor после и во время установки имплантатов, а также в период заживления. Показатели Periotest были зафиксированы три раза, и было определено среднее значение. Измерения с помощью Periotest проводились параллельно с Osstell.
- Рис. 5. Параллельное сверление кости
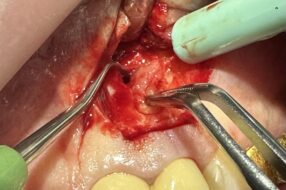
- Рис. 6. Установка имплантата — заметное скопление крови на поверхности имплантата благодаря гидрофильному покрытию
- Рис. 7. Идеальный торк при введении для достижения превосходной стабильности имплантата
Тестирование ISQ и использование Periotest для определения первичной и вторичной стабильности имплантатов могут показать значимый результат. По статистике, результаты обследования показывают повышение стабильности имплантатов через 6 недель после установки. Показатели Periotest увеличиваются в течение первых 6 недель от -3,64 до -4,74. Обследование, проведенное через 6 недель, выявило, что показатели Periotest сохранились на среднем уровне -4,75. Среднее значение ISQ для 16 имплантатов с установленными на них ортопедическими конструкциями через 6 недель составило 70,75 по сравнению со средним значением ISQ, равным 67,63, после установки имплантата. Сравнение биологических и клинических результатов в данной статье указывает на перспективы применения имплантатов с CaP-покрытием.
Литература
- Branemark P I, Hansson B O, Adell R, Breine U, Lindstrom J, Hallen O, Ohman A (1977). Osseointegrated implants in the treatment of the edentulous jaw. Experience from a 10-year period. Scand J Plast Reconstr Surg Suppl 16:1–132
- Esposito M, Murray-Curtis L, Grusovin M G, Coulthard P, Worthington H V (2007). Interventions for replacing missing teeth: different types of dental implants. Cochrane Database Syst Rev 4: CD003815. doi:10.1002/14651858
- Toyoshima T, Wagner W, Klein M O, Stender E, Wieland M, Al- Nawas B (2009). Primary stability of a hybrid self-tapping implant compared to a cylindrical non-self-tapping implant with respect to drilling protocols in an ex vivo model. Clin Implant Dent Relat Res. doi:10.1111/j.1708-8208.2009.00185.x
- Graf H L, Kn?fler W (1993). Bone reaction on biomaterials. VIII. Principles of bony regeneration under influence of foreign bodies. Z Zahn?rztl Implantol 9:62
- Kim K H, Ramaswamy N (2009). Electrochemical surface modification of titanium in dentistry. Dent Mater J. 28:20–36