Заболевания периимплантных тканей. Этиология. Патогенез
А. А. Глотова
врач-пародонтолог стоматологической клиники «ДЕНТиК ЛЮКС», член Российской пародонтологической ассоциации РПА (Краснодар)
Е. Н. Шастин
профессор РАЕ, руководитель стоматологической клиники «ДЕНТиК ЛЮКС» (Краснодар)
В статье описаны этиология, патогенез, клинические случаи заболевания периимплантных тканей. Приведены данные, свидетельствующие о связи заболеваний пародонта и дентальных имплантатов. Описана необходимость комплексного лечения заболеваний пародонта до момента имплантации.
Дентальные имплантаты произвели революцию в стоматологии, став новой надеждой для миллионов людей с отсутствующими зубами. После дебюта имплантатов в 1960-х годах мы добились больших успехов в понимании биологии остеоинтеграции. Однако с ростом числа установленных имплантатов также увеличивается количество поздних осложнений: мукозит, периимплантит, полная дезинтеграция.
По данным эпидемиологических исследований, через 10 лет периимплантит развивается примерно у 40 % пациентов, которым установлены имплантаты, в то время как мукозит в области имплантатов возникает примерно у 80 % пациентов. ( Berglund at al 2015 Clin Periodontolog & Implant Dentistry, Eke at al. J Dent Res 2012, Kassebaum at ol Dent Rec 2014).
Практически в каждой книге по имплантации вы найдете, что успешность этого метода лечения составляет на сегодняшний день при наличии современного оборудования и новейших технологий 98 % и выше, а выживаемость имплантатов в течение 10 лет составляет 95–97 %.
Гетербургское исследование Шведской популяции
Данное исследование (Journal on Dental Researelu 2015 Effectiveness of Implant Therapy analyzed in a Swedish population) на сегодняшний день самое крупное по поводу выживаемости имплантатов. Из 25 000 пациентов с установленными в 2003 году имплантатами было отобрано 4716 пациентов. Ранняя потеря имплантатов составила со стороны пациентов 4,4 % (121 пациент), со стороны имплантатов 1,4 % (154 имплантата). Через 9 лет после имплантологического лечения было оценено 596 пациентов, у которых было установлено 2367 имплантатов. Поздняя потеря составила со стороны пациентов 4,2 % (25 пациентов), со стороны имплантатов 2 % (47 имплантата). Общая потеря: пациенты — 7,6 %, имплантаты 3 %.
При оценке распространенности кариеса или пародонтита считается количество пациентов, имеющих эти заболевания, а не количество пораженных зубов, поэтому оценивать неудачу имплантации надо с точки зрения количества пациентов, а не имплантатов. Таким образом, выживаемость имплантатов в течение 10 лет составляет 93 %, а не 97 %, эти данные позволяют более реально оценивать результат и улучшить клинические работы.
Морфология
Строение периимплантных тканей включает в себя сходства и отличия с тканями пародонта. Самым главным отличием в строении тканей является наличие у зуба периодонтальной щели и связок по всей поверхности корня, а имплантат интегрируется с костной тканью посредством остеоинтеграции. Прилежащие к имплантату тканевые структуры могут быть разделены на периимплантную слизистую и альвеолярную кость.
Эпителиальные структуры
Периимплантные мягкие ткани содержат следующие эпителиальные структуры: оральный десневой эпителий, который направлен в полость рта; эпителий борозды, который направлен к поверхности имплантата, но не контактирует с ней; соединительный эпителий. Гистологическое строение окружающего имплант десневого эпителия имеет схожее строение с краевым пародонтом.
Соединительнотканные структуры
У имплантатов пучки надгребневых волокон расположены параллельно поверхности, а у естественных зубов коллагеновые волокна проходят в самых различных направлениях (Tomasi, 2013, Morphogenesis of the periimplantitis mucosa revisited an experimental study in humans).
Внутрикостная часть титановых имплантатов
Остеоинтеграция — прочное соединение между живой костной тканью и титановым имплантатом. Имплантат становится частью кости и передает в кость функциональные нагрузки.
Биологическая ширина и зубодесневой комплекс
В области имплантатов биологическая ширина также определяется как расстояние от наиболее выраженного коронкового выступа соединительного эпителия до альвеолярной кости, включающее эпителий (примерно 1 мм) и соединительнотканное прикрепление (около 1 мм). По аналогии с зубом зубодесневой комплекс дополнительно содержит участок импланто-десневой борозды (примерно 1 мм). Если это расстояние меньше, следует ожидать резорбцию окружающего имплантат гребня кости (Clin Oral Implants Res. 1991 Apr-Jun; 2(2):81-90 «The soft tissue barrier at implants and teeth» Berglundh T., Lindhe J., Ericsson I., Marinello CP., Liljenberg B., Thomsen P.).
Этиология
Согласно отчету шестого Европейского семинара по пародонтологии в 2008 году, мукозит и периимплантит признаны инфекционными заболеваниями, вызываемыми бактериями (Cindy& Meyle,2008, Consensus Report EP6). Мукозитом называют воспалительное поражение, которое ограничивается слизистой вокруг имплантата (рис. 1 а, б, в). Периимплантит — это патологическое состояние, возникающее в тканях, окружающих дентальные имплантаты, вызываемое микроорганизмами и характеризующееся воспалением тканей и потерей кости вокруг имплантата (рис. 2, 3 а, б).

Рис. 1 б. Периимплантный мукозит. Пациентка через 5 лет после фиксации мостовидного протеза обратилась с жалобами на дискомфортные ощущения в области имплантатов.
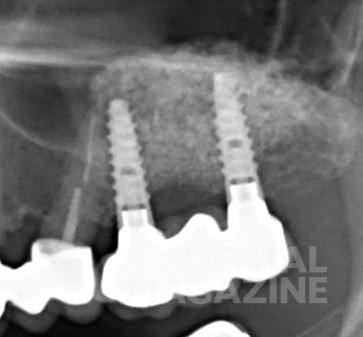
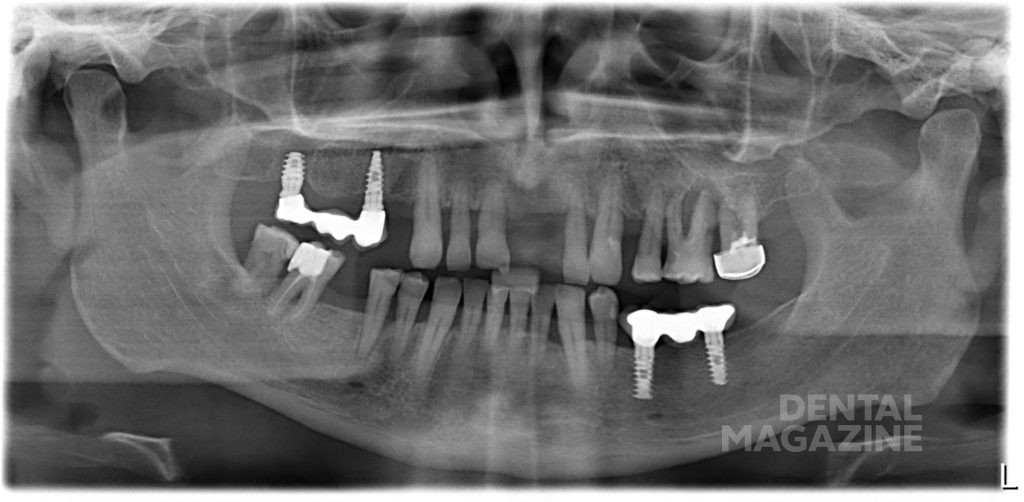
Рис. 1 в. Уровень костной ткани через 5 лет после фиксации металлокерамического мостовидного протеза. Отсутствует патологическая резорбция в области имплантатов, подтвержден диагноз «мукозит».
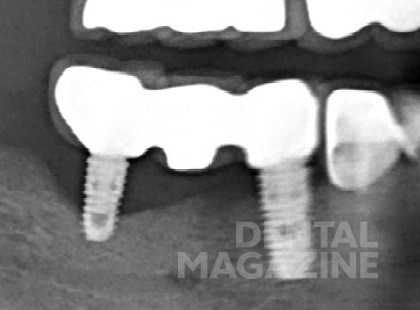
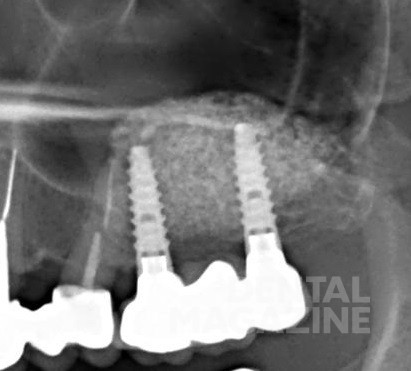
Рис. 2. Периимплантит. Резорбция кости на 2/3 длины имплантата через 3 года после установки имплантата.
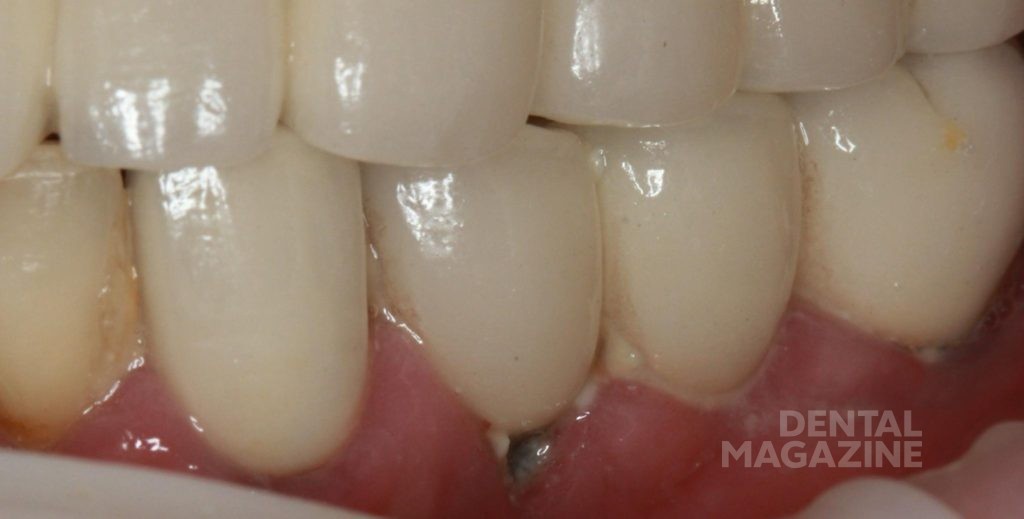
Рис. 3 а. Гигиена неудовлетворительная. Через 6 месяцев после постоянного протезирования диагностирован периимплантит.

Рис. 3 б. Гигиена неудовлетворительная. Через 6 месяцев после постоянного протезирования диагностирован периимплантит.
В последние годы в многочисленных экспериментальных и клинических исследованиях было установлено, что образование бактериальной биопленки является главным этиологическим фактором развития и прогрессирования периимплантита. К основным видам поддесневых бактерий относятся Peptostreptococcus micros, Fusobacterium nucleatum, Prevotella intermedia.
Воспаление десны и кости вокруг имплантатов развивается под действием грамотрицательной анаэробной микрофлоры, которая также ассоциируется с пародонтитом. При периимплантите обнаруживают большое количество пародонтальных патогенов, в частности бактерии красного комплекса (Porphyromonas gingivalis, Tannerella Forsythia, Treponema denticola), A. Actinimycetemcomitans, Prevotella intermedia. Предполагается, что микрофлора полости рта в момент имплантации влияет на формирование биопленки на поверхности имплантата. Соответственно, имеющиеся пародонтальные карманы в области естественных зубов служат резервуарами патогенных микроорганизмов, которые могут колонизировать установленные имплантаты.
Пародонтальные и периимплантатные карманы на одинаковой глубине зондирования у одного и того же пациента имеют схожий микробиологический состав. Таким образом, рационально заболевания пародонта необходимо предварительно лечить перед проведением имплантации в пределах протокола комплексной пародонтальной терапии.
Факторы риска
Большое значение для возникновения заболеваний вокруг имплантатов имеют факторы риска. К местным факторам относятся анатомические и клинические условия, способствующие колонизации патогенных бактерий: например, неудовлетворительная гигиена полости рта, глубокие десневые карманы, неблагоприятная конструкция протеза (рис. 4).
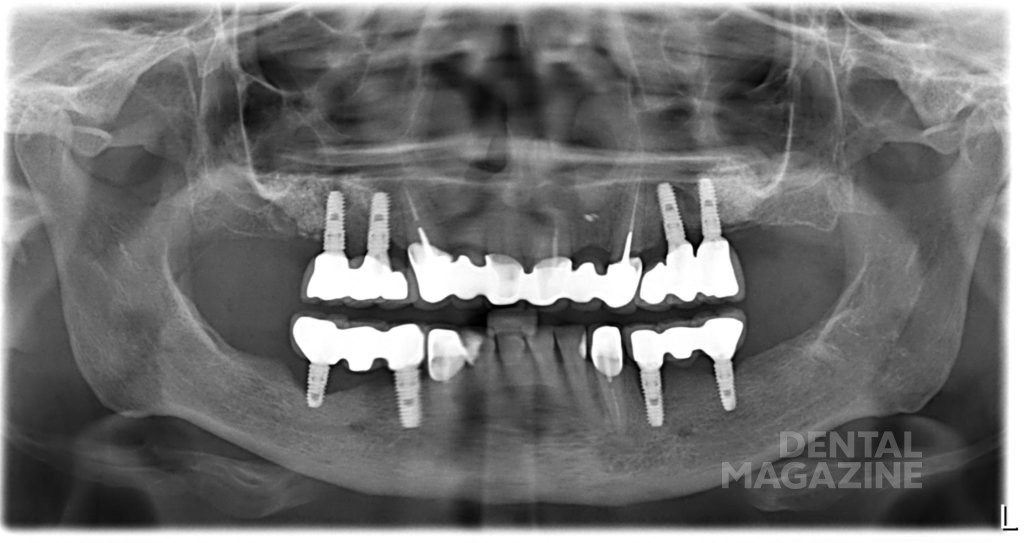
Рис. 4. Пациентка на плановом осмотре через 1 год после тотального протезирования. Гигиена неудовлетворительная, остатки пищи, мягкий зубной налет. Десна гиперемирована, отечна как в области своих зубов, так и в области имплантатов.
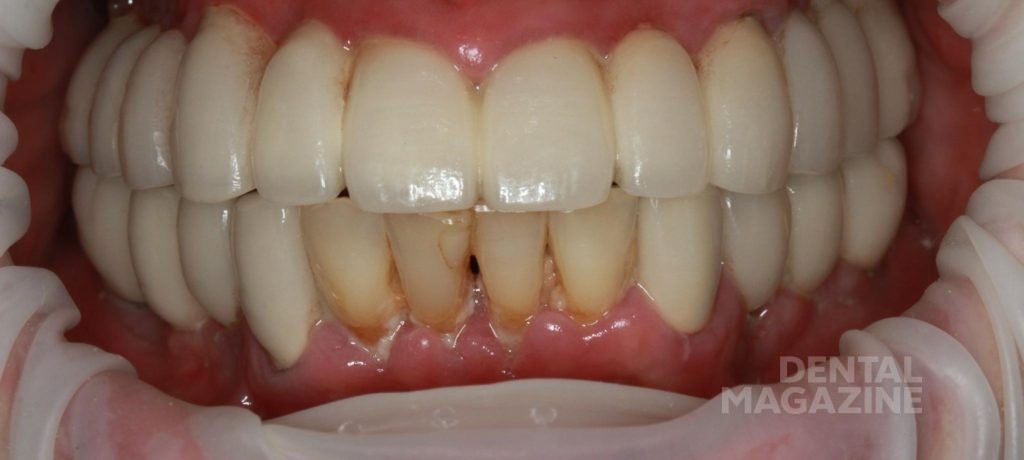
Рис. 4. Пациентка на плановом осмотре через 1 год после тотального протезирования. Гигиена неудовлетворительная, остатки пищи, мягкий зубной налет. Десна гиперемирована, отечна как в области своих зубов, так и в области имплантатов.
Общие факторы риска определяют ответ макроорганизма на микробную нагрузку — например, состояние здоровья пациента в целом, вредные привычки. Сочетание факторов риска может привести к выраженной реакции организма на воспаление, возникающее от бактериальной инфекции, что увеличит скорость резорбции кости при периимплантите.
Микрофлора полости рта колонизирует поверхности имплантатов и ортопедических конструкций так же, как традиционные несъемные протезы, поэтому самостоятельная гигиена полости рта имеет решающее значение для долгосрочного успеха имплантологического лечения. Скопление бактериального налета на придесневой поверхности протеза ведет к развитию мукозита, что клинически проявляется покраснением, отеком слизистой и кровоточивостью при зондировании десневой борозды. Отсутствие своевременного лечения приводит к дальнейшему прогрессированию воспалительного процесса, его распространению на костную ткань (рис. 5).
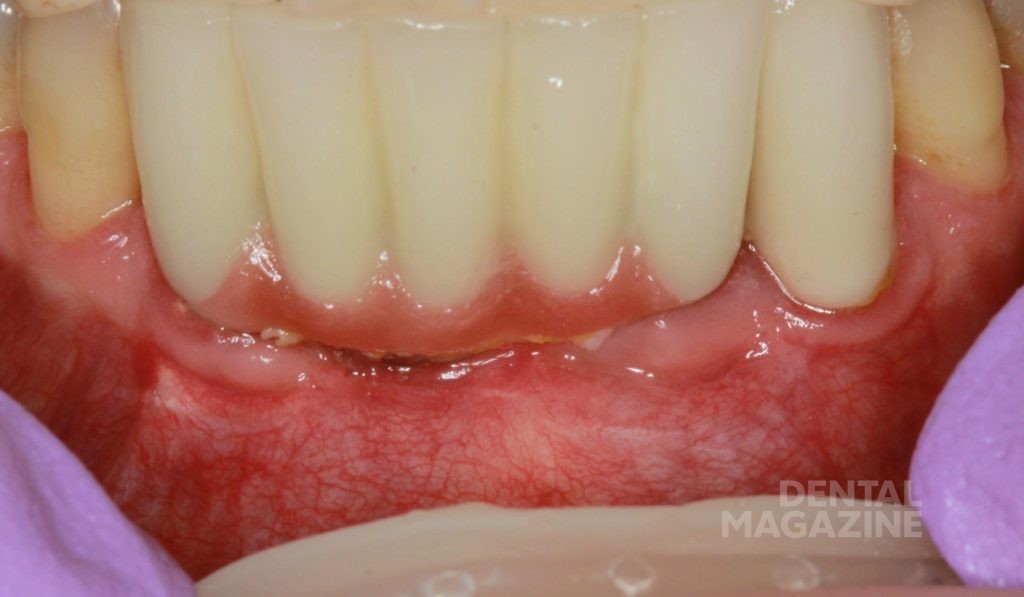
Рис. 5. Имплантаты в области 32-го, 42-го, 43-го зубов. Состояние десны через 2 месяца после постоянного протезирования. Неудовлетворительная гигиена в области металлокерамического протеза на имплантатах. Кровоточивость при зондировании.
При планировании имплантологического лечения нужно учитывать необходимость создания оптимальных условий для самостоятельной гигиены в области имплантатов. Следует помнить, что при отсутствии должного ухода периимплантит развивается очень быстро, даже если у пациента нет пародонтита в анамнезе.
Удаление всех зубов не позволяет полностью элиминировать пародонтопатогенные бактерии, так как они способны проникать в мягкие ткани; также при наличии членов семьи с диагнозом «пародонтит» происходит постоянное поступление пародонтопатогенной микрофлоры извне (через предметы гигиены, посуду, поцелуи).
Важное значение имеет интеграция мягких тканей к внутридесневым элементам ортопедических конструкций. Титановые и керамические абатменты способствуют формированию полосы прикрепления слизистой шириной 1,5 мм. К золоту и облицовочной керамике прикрепления почти не образуется, что повышает вероятность развития глубоких карманов. Кроме того, отмечается лучшая адгезия мягких тканей к относительно шероховатым поверхностям. Однако при обнажении более шероховатой поверхности в полости рта на ней быстрее скапливается бактериальный налет. Таким образом, при выборе системы имплантатов стоматолог сталкивается с определенной дилеммой. С одной стороны, нужно добиться лучшего прикрепления мягких тканей к внутридесневым структурам конструкции, а с другой — избежать избыточного скопления бактериального налета при обнажении в полости рта.
Существует мнение, что избыточная окклюзионная нагрузка может вызвать убыль кости вокруг имплантатов. Многие авторы изучали взаимосвязь между нагрузкой на имплантат и резорбцией краевой кости. Большинство подобных исследований проводилось на животных моделях в течение 12–15 лет. Оказалось, что нагрузка на имплантаты не сопровождается резорбцией кости вокруг них. Напротив, степень минерализации кости, непосредственно контактирующей с имплантатом, повышается по сравнению с имплантатом, который не испытывает такой нагрузки. Таким образом, избыточная нагрузка на имплантаты в долгосрочном периоде может привести исключительно к биомеханическим повреждениям (раскручивание винта, расцементировка коронки, перелом абатмента, перелом имплантата), а костная резорбция вокруг интегрированных имплантатов связана только с бактериальной инфекцией.
Курение сигарет должно рассматриваться как потенциальный фактор риска, т. к. табачный дым напрямую влияет на местный иммунитет в полости рта. Происходит снижение хемотаксиса и фагоцитоза нейтрофилов, стимуляция противовоспалительных цитокинов, активация поддесневых анаэробов, это все может стать причиной ранних и поздних осложнений после установки имплантатов.
Большую роль в успехе имплантологического лечения играет профессионализм, теоретические знания и мануальные навыки врача. К сожалению, в связи с популяризацией имплантации у врачей сложилось мнение, что установка имплантатов достаточно простая манипуляция, не требующая больших теоретических знаний и мануальных навыков. Согласно последним исследованиям в области изучения периимплантита, в более чем 90 % случаев это заболевание вызвано плохим планированием, неоптимальным лечением.
Патогенез
Непосредственный контакт между скоплением микроорганизмов и окружающими имплантат мягкими тканями приводит к воспалению и увеличению глубины зондирования аналогично процессам, происходящим в области естественных зубов. Экспериментальные исследования подтверждают схожую воспалительную реакцию вокруг зубов и имплантатов в ответ на действия бактериальных раздражителей. В обоих случаях поражение локализуется в области края десны. Прогрессирование воспалительного процесса и инфильтрация тканей крупными лимфоцитами ведет к резорбции костной ткани. Клетки, продуцирующие эластазу, в большем количестве встречаются при периимплантите, чем при пародонтите, что указывает на более быстрое прогрессирование повреждения кости вокруг имплантатов.
По мере скопления налета очаг поражения тканей вокруг имплантата распространяется в апикальном направлении. Воспалительный инфильтрат включает в себя плазмоциты, макрофаги, лимфоциты и большое количество полиморфноядерных лейкоцитов. Более того, именно увеличение количества полиморфноядерных лейкоцитов может объяснить повышение концентрации эластазы при периимплантите по сравнению с пародонтитом. Воспалительный инфильтрат при периимплантите непосредственно распространяется на альвеолярную кость и проникает в костномозговые пространства. Это обстоятельство отличает характер воспаления при периимплантите, поскольку при пародонтите воспалительный инфильтрат отделен от костной ткани плотным соединительным слоем толщиной около 1 мм. При периимплантите и пародонтите обнаруживаются цитокины, повышающие активность остеокластов, однако при периимплантите превалирует интерлейкин-1А, в то время как при пародонтите большее влияние оказывает туморнекротизирующий фактор альфа. Важное значение при патогенезе развития процесса имеет отсутствие у имплантата периодонтальной щели и связки. Зуб обладает отличным кровоснабжением и сильным иммунитетом, в связи с этим организм способен сопротивляться инфекции и пародонтит длится годами — от момента возникновения поддесневой инфекции и до момента полной потери окружающих зуб тканей может пройти 15–20 лет. У имплантата из-за отличия в строении и патогенезе, описанном выше, полная дезинтеграция может наступить в течение 3–5 лет от момента возникновения периимплантита (рис. 6).
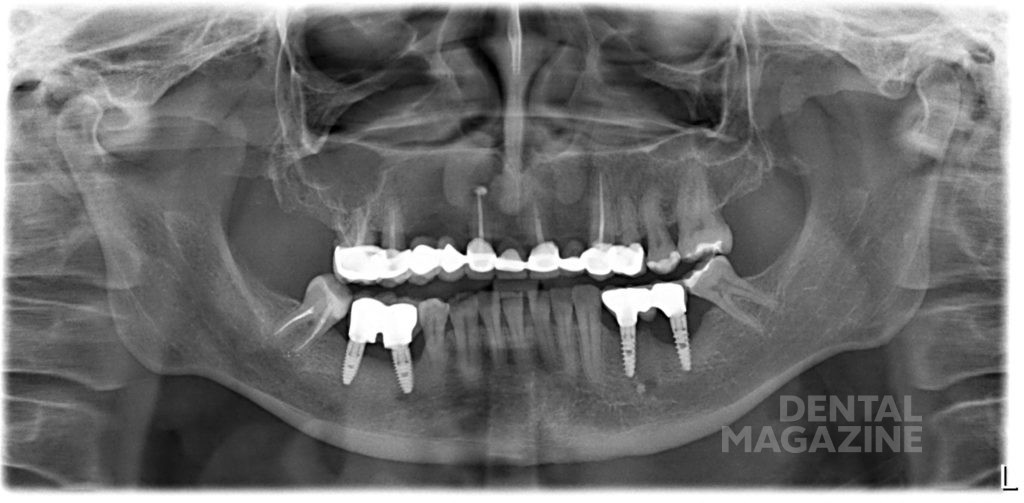
Рис. 6 б. Пациент жалоб не предъявляет. На плановом осмотре с рентген-контролем через 2 года после фиксации выявлено блюдцеобразное разряжение костной ткани.
Клинический случай № 1
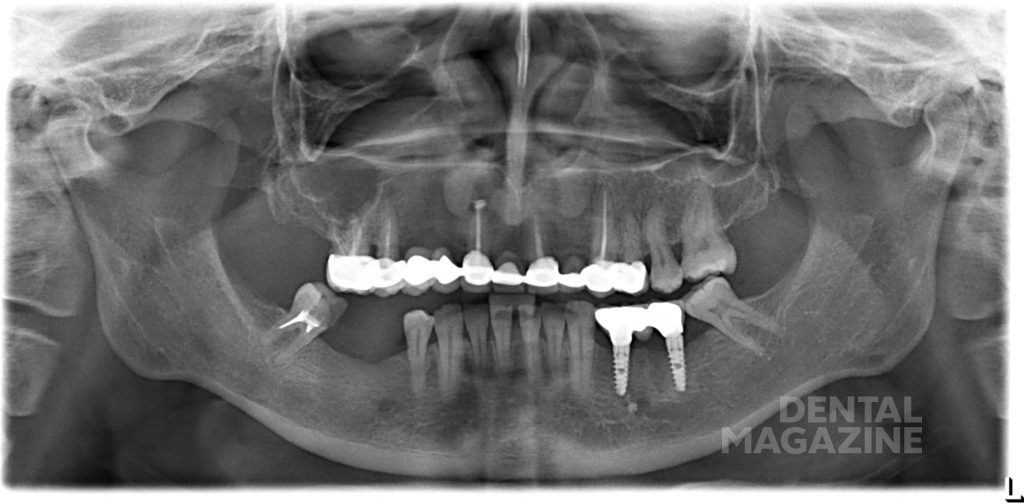
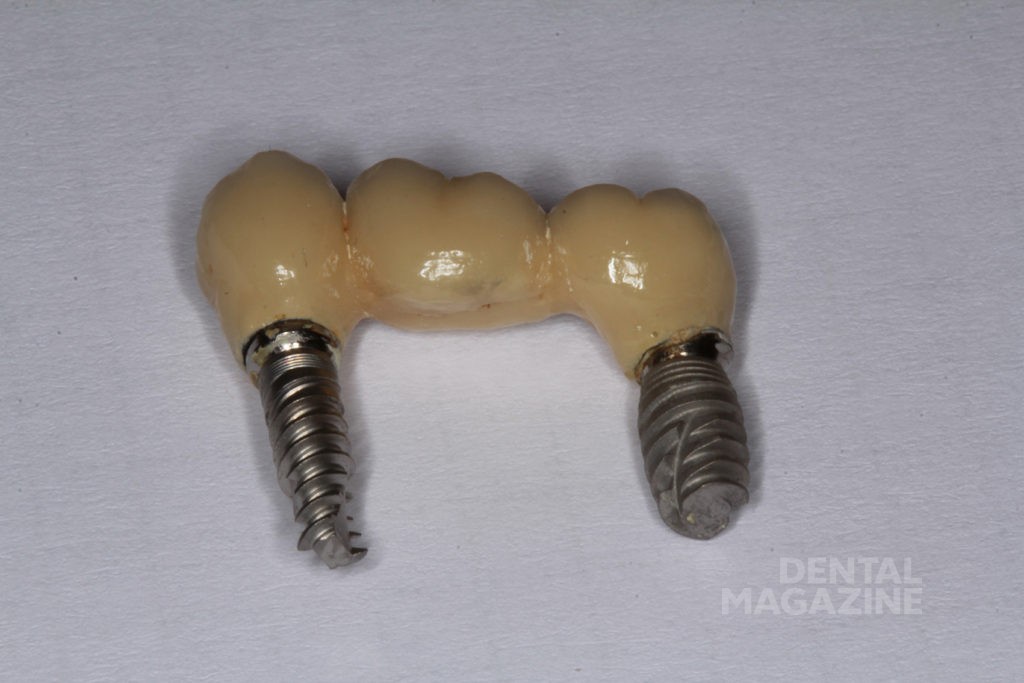
Имплантаты в области 15-го, 17-го зубов установлены 7 лет назад. Пациент игнорировал плановые осмотры, диспансерное наблюдение, периодически появлялся в клинике для удаления зубов, при этом отказываясь от лечения пародонтита. Все отсутствующие зубы удалены по пародонтологическим показаниям. При каждом визите проводилась беседа о рисках потери своих зубов и имплантатов. Пациент с хроническим нелеченым пародонтитом тяжелой степени тяжести обратился в клинику с жалобами на подвижность мостовидного протеза 15–17. Удален мостовидный протез 15–17 вместе с имплантатами в связи с полной дезинтеграцией.
Врач должен осознавать, что «имплантаты тоже болеют» и главное — объяснять это пациенту. У имплантатов нет иммунитета, в отличие от естественных зубов, поэтому после имплантологического лечения необходима активная диспансеризация пациентов. Достаточно опрометчиво, зная о заболеваниях периимплантных тканей, давать пациентам пожизненную гарантию на имплантаты или говорить, что за имплантатами нет особого ухода.
Вся проблема при лечении периимплантита заключается в том, что отсутствуют долгосрочные клинические наблюдения различных методов лечения. Им просто неоткуда взяться, потому что большинство врачей, не понимая полностью этиологию и особенности патогенеза, единственным методом лечения периимплантита считают наиболее простой и предсказуемый путь решения проблемы — удаление имплантата. Врач, столкнувшись с такой проблемой, должен понимать, что, не выяснив причины возникновения периимплантита и не устранив их, нет никакой гарантии, что после удаления и установки нового имплантата периимплантит не возникнет вновь.
Несколько десятилетий назад многие врачи придерживались мнения, что пародонтит не лечится и единственный способ лечения — удаление («нет зуба — нет проблем»). Периимплантит как заболевание переживает сейчас точно такой же период — «нет имплантата — нет проблем». Если мы не знаем, как лечить, это еще не значит, что заболевание не лечится.
В следующих статьях мы разберем подробно классификацию заболеваний периимплантных тканей, диагностику, консервативное и хирургическое лечение, диспансерное наблюдение.
- JADA 2014; 145 (7):704-713
- A Proposed Classification for Peri-Implantitis; Froum & Rosen; Int J. Periodontics Restorative Dent 2012; 32:533–540.
- Mombelli A., Lang NP. Antimicrobial treatment of peri-implant infections. Clin. Oral Implants Res. 1992; 3:162–168.
- Schwarz F. et al. (2006). Influence of different treatment approaches on nonsubmerged and submerged healing of ligature-induced peri-implantitis lesions: an experimental study in dogs. Journal of Clinical Periodontology Aug. 2006; 33 (8):584–595.
- Renvert S. Topical minocycline microspheres versus topical chlorhexidine gel as an adjunct to mechanical debridement of incipient peri-implant infections: a randomized clinical trial. J. Clin. Periodontol. May 2006; 33 (5): 362–369.
- Schwarz F. et al. (2006 a). Nonsurgical treatment of moderate and advanced peri-implantitis lesions: a controlled clinical study. Clinical Oral Investigations 10, 279–288.
- Schwarz F. et al. (2006). Influence of different treatment approaches on nonsubmerged and submerged healing of ligature-induced peri-implantitis lesions: an experimental study in dogs. Journal of Clinical Periodontology Aug. 2006; 33(8):584–595.
- Renvert S. (2008), Nonsurgical treatment of peri-implant mucositis and peri-implantitis: a literature review. J. Clin. Periodontol. Sept. 2008; 35 (8 Suppl):305–315.
Глотова Алла Андреевна, врач-пародонтолог стоматологической клиники «ДЕНТиК ЛЮКС», Россия, Краснодар
Glotova A.A., periodontist of the dental clinic «Dentik Lux», Russia, Krasnodar
Шастин Евгений Николаевич, руководитель стоматологической клиники «ДЕНТиК ЛЮКС», Россия, Краснодар
Shastin E.N., Head of the dental clinic «Dentik Lux», Russia, Krasnodar
350015, Россия, Краснодар, ул. Северная, 400 / ул. Янковского, 170
Тел. +7 (861) 210-10-03
e-mail: [email protected]
Peri-implant tissue diseases. Etiology. Pathogenesis.
Аннотация. Целью статьи является описание причин возникновения заболеваний периимплантных тканей и патогенез развития. Автор описывает клинические исследования на эту тему и дает ссылки на статьи, чтобы врач мог подробнее изучить этот вопрос самостоятельно.
Annotation. The purpose of the article is to describe the causes of diseases of the peri-implant tissue and the pathogenesis of development. The author describes clinical studies on this topic and provides links to articles so that the doctor can study this issue in more detail on his own.
Ключевые слова: мукозит; периимплантит; периимплантные ткани; биологическая ширина; импланто-десневая борозда; патогенез периимплантита.
Keywords: mucositis; periimplantitis; peri-implant tissues; biological width; implant-gingival sulcus; peri-implant pathogenesis.
Литература