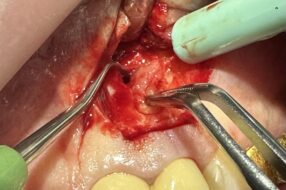
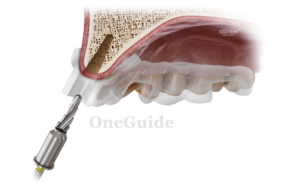
Современный подход к антибактериальной обработке при лечении осложненного кариеса зубов со сложной анатомической формой корневых каналов
Б. Р. Шумилович
д. м. н., профессор кафедры стоматологии ИДПО ВГМА им. Н. Н. Бурденко, врач высшей категории
А. Е. Толоконикова
аспирант кафедры стоматологии ИДПО ВГМА им. Н. Н. Бурденко
В. А. Кунин
д. м. н., профессор, заведующий кафедрой пропедевтической стоматологии ВГМА им. Н. Н. Бурденко, проректор по НИДИ ВГМА им. Н. Н. Бурденко
Е. В. Кадменская
аспирант кафедры терапевтической стоматологии СГМУ им. В. И. Разумовского
Оценка основных статистических показателей работы многих специализированных стационаров Российской Федерации за последний период применительно к больным с острой одонтогенной инфекцией показывает, что произошло заметное увеличение их общей численности, выросло процентное соотношение числа госпитализированных больных, увеличилось количество больных с осложненными формами течения.
Как свидетельствуют литературные источники, причинами такого увеличения количества больных и возрастания тяжести клинического проявления одонтогенной инфекции являются, во-первых, значительное изменение микрофлоры, вызывающей воспалительные заболевания одонтогенной природы (за счет увеличения роли сапрофитной или условно патогенной флоры); во-вторых, как следствие первого фактора, снижение лечебной эффективности применяемых в стоматологии антимикробных средств широкого спектра действия, немаловажным здесь представляется необоснованное массовое местное применение антибиотиков; в-третьих, заметное увеличение количества пациентов, имеющих «фоновые» заболевания, отягощенный аллергологический статус, и, наконец, в-четвертых, несовершенство методов лечения осложненного кариеса, в результате чего открытые, дренируемые очаги инфекции превращаются в закрытые, недренируемые.
Кроме того, определенное значение имеет своеобразие применяемых способов лечения эндодонтических больных, характеризующихся многократностью внедрения различного стоматологического инструментария в инфицированные твердые ткани зуба.
В настоящее время доказана идентичность флоры дентина корневых каналов и очагов острой одонтогенной инфекции.
К сожалению, при активно протекающих воспалительных процессах (хронический гангренозный пульпит, хронический гранулирующий и гранулематозный периодонтит), характеризующихся высокой вирулентностью и ведущей ролью неклостридиальной анаэробной микрофлоры, стандартные методы биомеханической обработки корневых каналов недостаточно эффективны, особенно в многокорневых зубах и зубах со сложной анатомией корневого канала.
Несомненно, что такое положение дел ставит перед стоматологами задачу постоянного усовершенствования существующих методов эндодонтического лечения, которая на сегодняшний день достаточно успешно решается. Это касается как механической обработки каналов (применение ротационных технологий, постоянное совершенствование никель-титанового инструмента, реципрокный эндодонтический инструментарий, самоадаптирующиеся файлы и мн. др.), так и медикаментозной подготовки канала и его обтурации (создание систем трехмерной обтурации и т. д.). На высокотехнологическом уровне проводится контроль качества проведения различных этапов эндолечения (операционный микроскоп, компьютерная томография и т. д.).
Учитывая вышесказанное, а также с развитием физических факторов антибактериального воздействия, в частности, лазерных, ультразвуковых, озонотерапии и т. д., в современной стоматологической практике определились возможности получения оптимальных результатов лечения осложненного кариеса. В связи с этим несомненный интерес для клиницистов представляет предложенный для практической стоматологии метод антибактериальной обработки корневых каналов с использованием газообразного озона.
Прибор является генератором газообразного озона из атмосферного воздуха при помощи электрического тока высокого напряжения. Газообразный озон представляет собой трехатомный кислород, который при контакте с атмосферным воздухом разлагается на двух- и одноатомный. Одноатомный кислород является сильнейшим окислителем, превосходящим по силе гипохлорит натрия (табл. № 1), и убивает все известные вирусы и бактерии, что делает его наиболее эффективным антибактериальным средством в клинической стоматологии, имеющимся на сегодняшний день.
Таблица № 1. Сравнительные окислительные потенциалы распространенных антибактериальных средств при 25 °C
Антибактериальные средства |
Потенциал (Вольт) |
| Фтор (F2) | 2.87 |
| Озон (O3) | 2,07 |
| Перекись водорода(H2O2) | 1,78 |
| Перманганат калия(KМnO4) | 1,70 |
| Гипобромистая кислота (HОBr) | 1,59 |
| Гипохлористаякислота (HОCl) | 1,49 |
| Хлор (C12) | 1,36 |
| Двуокись хлора(CIO2) | 1,27 |
| Кислород (O2) | 1,23 |
| Хромовая кислота(H2CrO4) | 1,21 |
| Бром (Br2) | 1,09 |
| Азотная кислота(HNO3) | 0,94 |
| Иод (I2) | 0,54 |
Озон открыл в 1785 г. Ван Марум, в 1885 г. вышла первая медицинская публикация д-ра К. Кенворти «Озон». Массовое применение в медицине берет свое начало с 1898 г. когда в Берлине открылся первый институт кислородной терапии. В 1930 г. д-р Е. А. Фиш, швейцарский дантист, впервые применил озон в стоматологии и написал об этом несколько печатных работ. Современный этап озонотерапии в стоматологии начинается с 2002 г., когда Брам ван Дик выпустил свой аппарат OziCare — настольный генератор озона, предназначенный для стоматологии.
Механизм антибактериального действия озона заключается в избирательном воздействии одноатомного кислорода на клеточную мембрану бактерий, особенно анаэробных. Низшие организмы, в отличие от более высокоорганизованных, не вырабатывают ферментную оболочку клеточной мембраны, которая предотвращает реакцию с озоном, следовательно, разрушается клеточная мембрана (целлиз — разрыв клеточной мембраны) и происходит гибель микроорганизма.
За период 2009—2011 гг. на кафедре стоматологии ИДПО и кафедре пропедевтической Воронежской государственной медицинской академии им. Н. Н. Бурденко было пролечено 106 пациентов с различными нозологическими формами осложненного кариеса, имеющих сложную анатомию корневых каналов. Сложной анатомией считались превышение угла изгиба корневого канала более чем на 300, S-образные каналы, C-shape-каналы, каналы в виде песочных часов, внутриканальная резорбция, третьи моляры, повторное эндодонтическое лечение.
Из них 10 с диагнозом «хронический фиброзный пульпит», 37 — «хронический гангренозный пульпит», 20 — «хронический фиброзный периодонтит» и 39 с диагнозом «хронический гранулирующий периодонтит». Соблюдался стандартный протокол эндодонтического лечения — механическая обработка (создание «ковровой дорожки» + основная обработка ротационным инструментом с соблюдением всех необходимых требований), химическая обработка (3%-ный стабилизированный раствор гипохлорита натрия + 17%-ный раствор ЭДТА + дистиллированная вода по общепринятой схеме) и последующая обработка газообразным озоном по следующей методике:
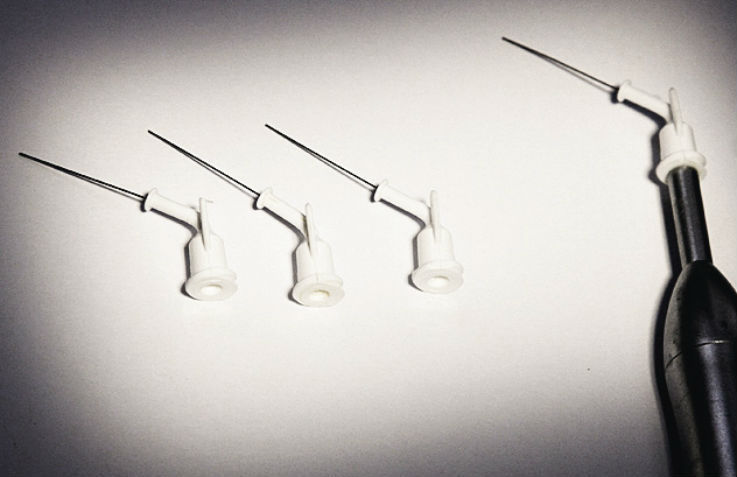
- насадка типа ENDOTIP (рис. 1);
- если в канале обнаруживается апикальное кровотечение, газообразный озон использовался для коагуляции;
- перед воздействием канал высушивается бумажными штифтами;
- использовался режим экспозиции «24 сек.»;
- газ в канал вводится шагом 2-5;
- после дезинфекции канал сразу же обтурировался либо термогуттаперчей на носителе с использованием силера на основе полимера, либо методом латеральной компакции гуттаперчи с использованием силера на основе полидиметилсилоксана.
Результаты проведенного лечения представлены на рисунках 2—9.
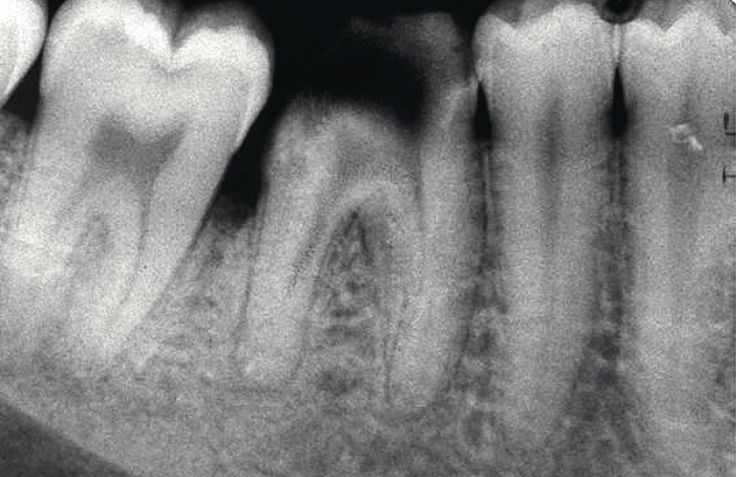
Рис. 2а. Зуб 4.6, Ds: хронический гангренозный пульпит 4.6 («сходящиеся» корневые каналы): исходная ситуация.
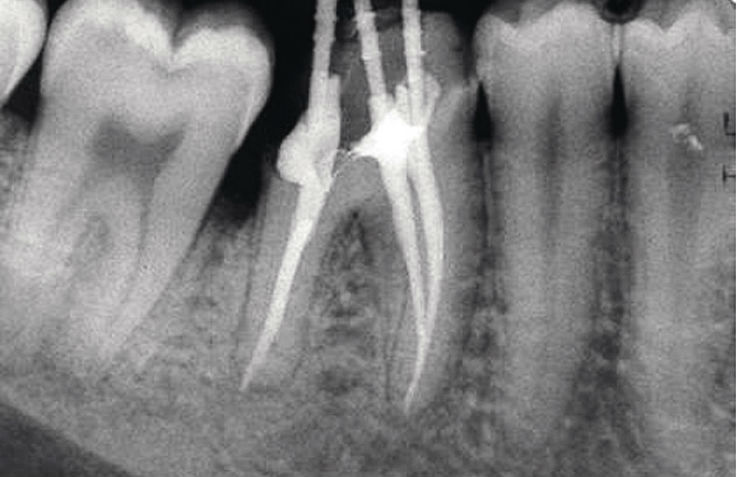
Рис. 2б. Зуб 4.6, Ds: хронический гангренозный пульпит 4.6 («сходящиеся» корневые каналы): результат лечения.
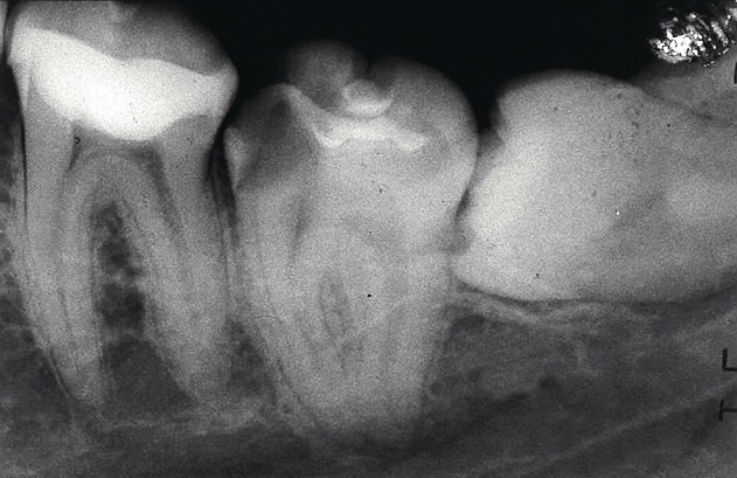
Рис. 3а. Зуб 3.7, Ds: хронический гангренозный пульпит 3.7 (корневые каналы в форме песочных часов): исходная ситуация.
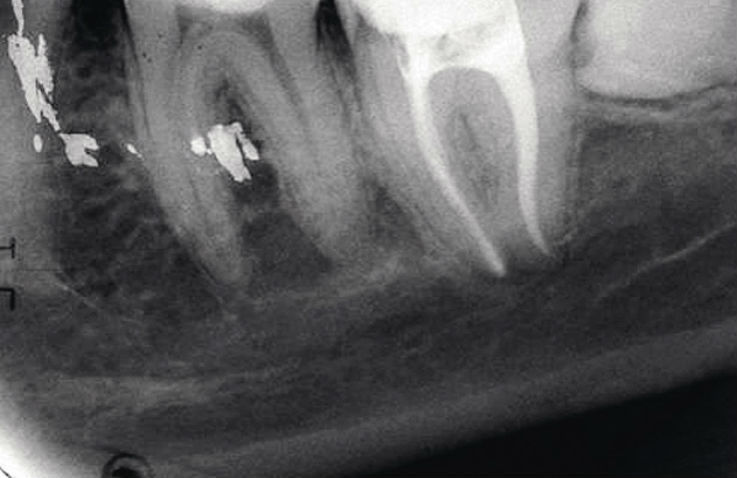
Рис. 3б. Зуб 3.7, Ds: хронический гангренозный пульпит 3.7 (корневые каналы в форме песочных часов): спустя 6 мес. после лечения.
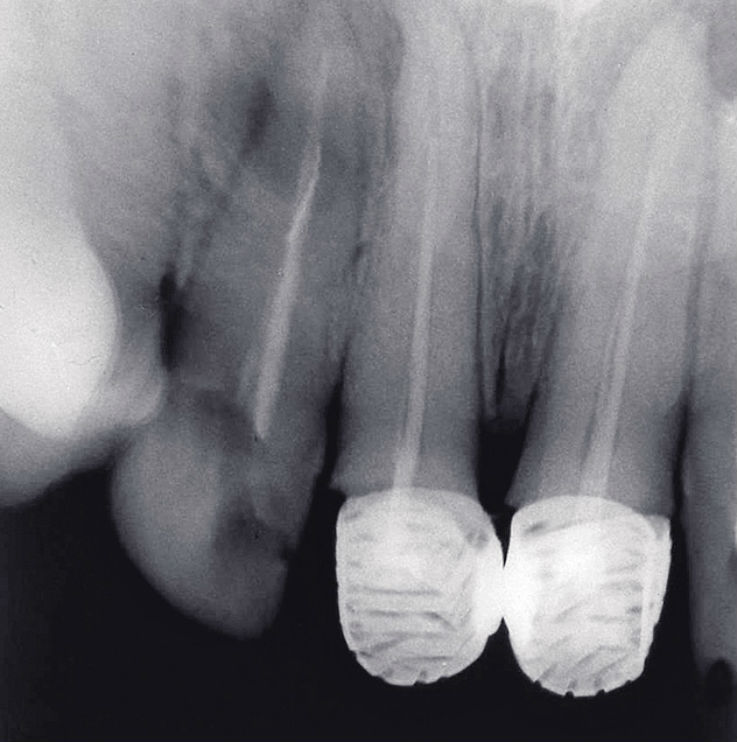
Рис. 4а. Зубы 1.2, 1.1, 2.1, Ds: хронический фиброзный периодонтит 1.1, 2.1, хронический гранулирующий периодонтит 1.2 (повторное эндодонтическое лечение): исходная ситуация.
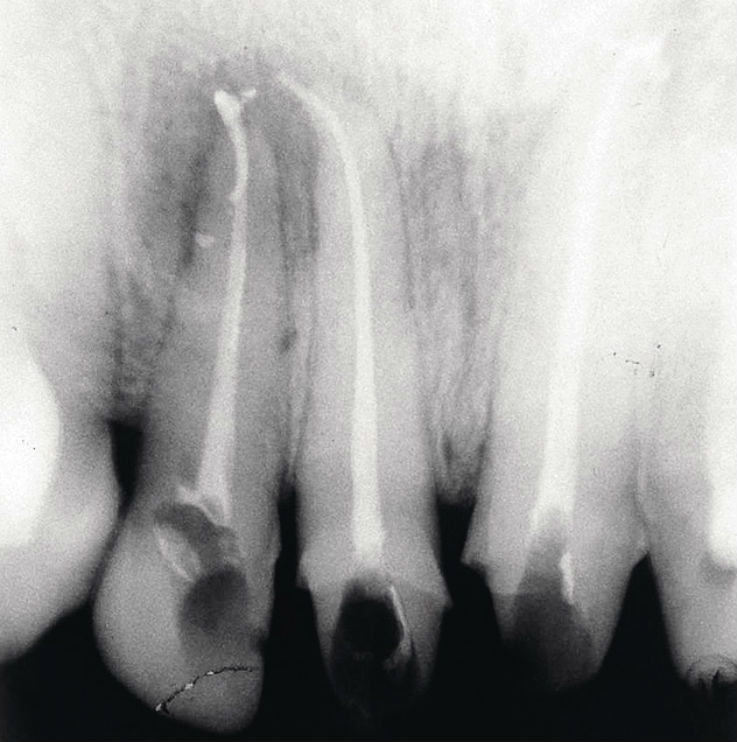
Рис. 4б. Зубы 1.2, 1.1, 2.1, Ds: хронический фиброзный периодонтит 1.1, 2.1, хронический гранулирующий периодонтит 1.2 (повторное эндодонтическое лечение): спустя 1 мес. после лечения.
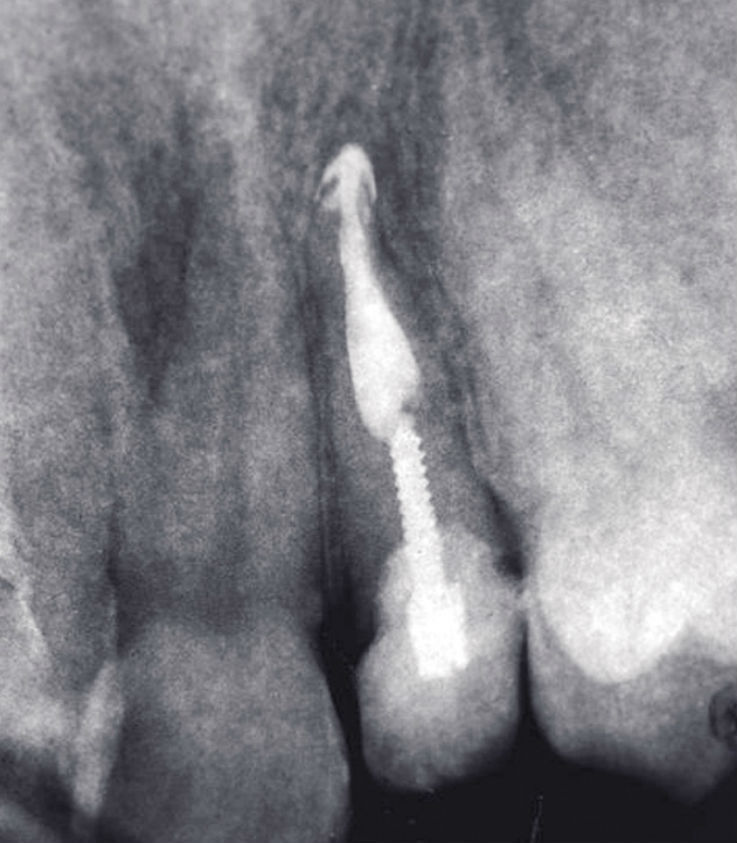
Рис. 5. Зуб 1.2, Ds: хронический гранулирующий периодонтит 1.2 (внутренняя резорбция). Спустя 6 мес. после лечения.

Рис. 6а. Зуб 3.7, Ds: хронический фиброзный периодонтит 3.7 (повторное эндодонтическое лечение): исходная ситуация.
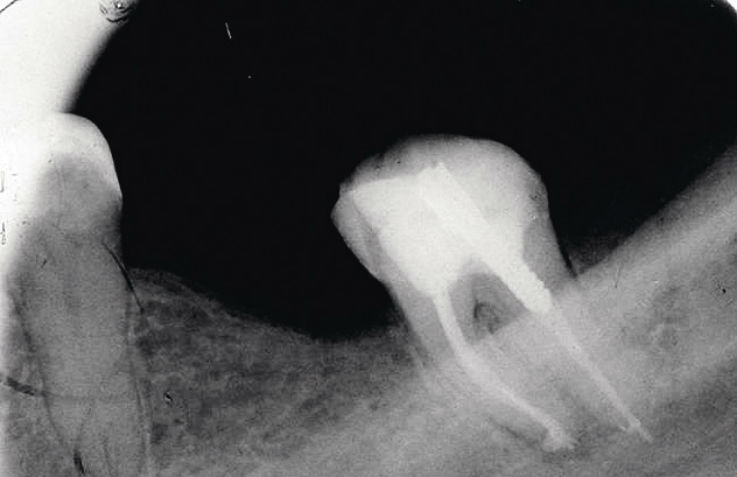
Рис. 6б. Зуб 3.7, Ds: хронический фиброзный периодонтит 3.7 (повторное эндодонтическое лечение): результат лечения.
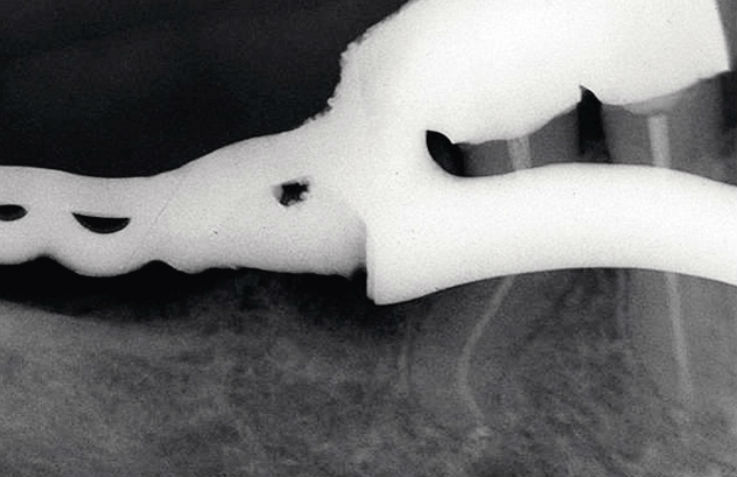
Рис. 7. Зуб 3.5, Ds: хронический гангренозный пульпит 3.5 (корневой канал S-образной формы). Спустя 12 мес. после лечения.

Рис. 8а. Зуб 3.7, Ds: хронический фиброзный периодонтит 3.7, (повторное эндодонтическое лечение, резорбция корней): исходная ситуация.
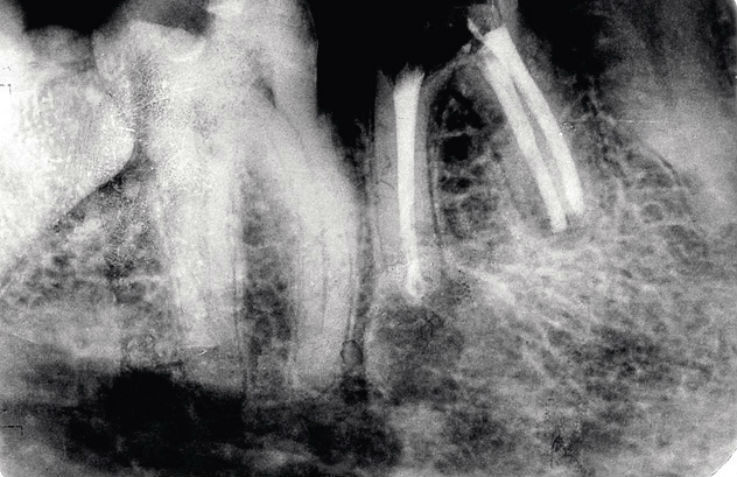
Рис. 8б. Зуб 3.7, Ds: хронический фиброзный периодонтит 3.7, (повторное эндодонтическое лечение, резорбция корней): результат лечения.
За весь период клинических наблюдений нами не было выявлено ни одного случая обострения исследуемых форм осложненного кариеса.
Особого внимания, на наш взгляд, заслуживают результаты проводимых параллельно с эндодонтическим лечением микробиологических исследований неклостридиальной анаэробной флоры корневого дентина. При их проведении использовались методы экспресс-диагностики количественного определения и идентификации выделенных культур по В. В. Хазановой.
В таблице № 2 представлен исходный видовой состав анаэробной микрофлоры корневого дентина, а также удельный вес вида микроорганизма от общего бактериального обсеменения в зависимости от диагноза.
Таблица № 2. Исходный видовой состав и удельный вес анаэробной микрофлоры корневого дентина (%)
Видмикроорганизма |
Нозологическая форма осложненного кариеса |
|||
| Хроническийфиброзный
пульпит |
Хроническийгангренозный
пульпит |
Хроническийфиброзный
периодонтит |
Хроническийгранулирующий
периодонтит |
|
| Peptostreptococcus | 4,3 % | 5,7 % | 8,2 % | 1,3 % |
| Bacillus cereus | 8,7 % | 5,7 % | 10,2 % | 14,2 % |
| Bacteroidisfragilis | 4,3 % | 10,0 % | 10,2 % | 7,7 % |
| Bacteroidismelaninogenicus | – | 8,6 % | 6,1 % | 9,6 % |
| Fusobacteriumnucleatum | – | 7,3 % | 10,2 % | 11,5 % |
| ИТОГО(% от ОМЧ) | 17,3 % | 37,3 % | 44,9 % | 45,3 % |
Как следует из вышеприведенных данных, изменение качественного состава анаэробной флоры по мере нарастания тяжести процесса идет по пути уменьшения содержания пептострептококков и увеличения содержания бактероидов и фузобактерий. Также большое значение для характеристики качественного состава микрофлоры имеет способность микроорганизмов к объединению в микробные ассоциации, вследствие чего значительно повышается их вирулентность. Эта способность увеличивается в первую очередь по мере нарастания тяжести процесса и во вторую очередь зависит от вида микроорганизма. У анаэробов и дрожжевых грибов она проявляется в наибольшей степени.
Следующим этапом работы явилось микробиологическое исследование дентина после традиционной биохимической обработки корневых каналов и после дополнительной обработки газообразным озоном. Сравнительные данные по высеваемости микроорганизмов представлены в таблице № 3.
Таблица № 3. Сравнительные данные по высеваемости анаэробных микроорганизмов после традиционной биохимической обработки и дополнительной озонотерапии (КОЕ / сектор II)
Видмикроорганизма |
Нозологическая форма осложненного кариеса |
|||||||
| Хроническийфиброзный
пульпит |
Хроническийгангренозный
пульпит |
Хроническийфиброзный
периодонтит |
Хроническийгранулирующ.
периодонтит |
|||||
| Трад. | Prozone | Трад. | Prozone | Трад. | Prozone | Трад. | Prozone | |
| Peptostreptococcus | оченьмного | нетроста | оченьмного | нетроста | 100—150 | нетроста | 20—30 | нетроста |
| Bacillus cereus | оченьмного | нетроста | 30—60 | нетроста | 20—30 | нетроста | 20—30 | нетроста |
| Bacteroidisfragilis | 30—60 | нетроста | 100—150 | нетроста | оченьмного | 1—5 | оченьмного | 3—8 |
| Bacteroidismelaninogenicus | – | – | 30—60 | 1—3 | 100—150 | нетроста | 100—150 | нетроста |
| Fusobacteriumnucleatum | – | – | 100—150 | нетроста | оченьмного | нетроста | оченьмного | 3—8 |
К сожалению, как видно из результатов микробиологических исследований, общепринятая подготовка корневых каналов даже при использовании стабилизированного раствора гипохлорита натрия и полного соблюдения протокола эндодонтического лечения не гарантирует бактериальной «чистоты» операционного поля. Особенно это касается анаэробной флоры при хроническом гангренозном пульпите и хроническом гранулирующем периодонтите. Выражение «еще ни один стоматолог в мире никогда не запломбировал стерильного корневого канала» актуально и на сегодняшний день, и дополнительная возможность эффективного антимикробного воздействия, несомненно, должна получить активную поддержку клиницистов.
Таким образом, анализируя данные таблицы, можно сделать вывод, что озон обладает ярко выраженным бактерицидным эффектом по отношению к большинству видов обнаруженной микрофлоры. Наибольшей резистентностью обладают бактероиды и фузобактерии, однако при дальнейшем высеивании и выделении чистой культуры их роста не обнаруживалось, что свидетельствует об их крайне низкой вирулентности.
Мы взяли за критерий оценки рост микроорганизмов на II секторе по Goild, так как, по литературным данным, именно в этом состоянии микроорганизмы еще способны вегетировать в естественных условиях корневого канала и служить этиологическим фактором неудовлетворительного эндодонтического лечения, которое, конечно же, не ведет к процветанию вашей стоматологической практики.
Кроме того, дополнительно принимая во внимание возможность применения представленного метода в кариесологии и пародонтологии, его способность насыщать ткани кислородом, а также учитывая разумную ценовую политику лечебных учреждений, мы выражаем твердую уверенность в том, что включение озонотерапии в повседневную клиническую деятельность позволит значительно повысить профессиональный уровень врача-стоматолога, что, в свою очередь, несомненно, приведет к повышению качества оказания стоматологической помощи и уменьшению количества рецидивов.